Hallo zusammen
Diese Woche hatte ich noch keine Zeit in den Wald zu gehen. Aber im Garten gab es zwei schöne Samthäubchen, damit war ich dann auch zufrieden:

1: Conocybe albipes
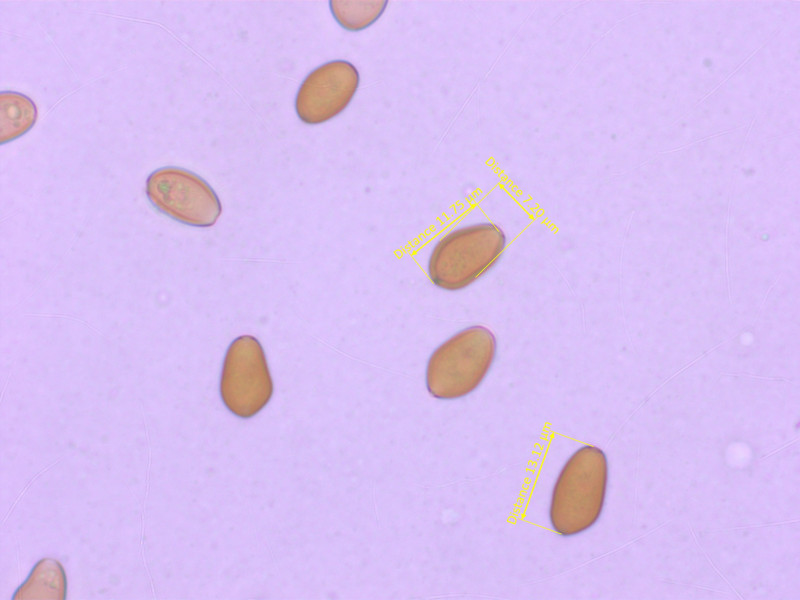
Die Sporen sind zum Teil recht unregelmässig geformt, deshalb war ich bei der Bestimmung anfangs unsicher.
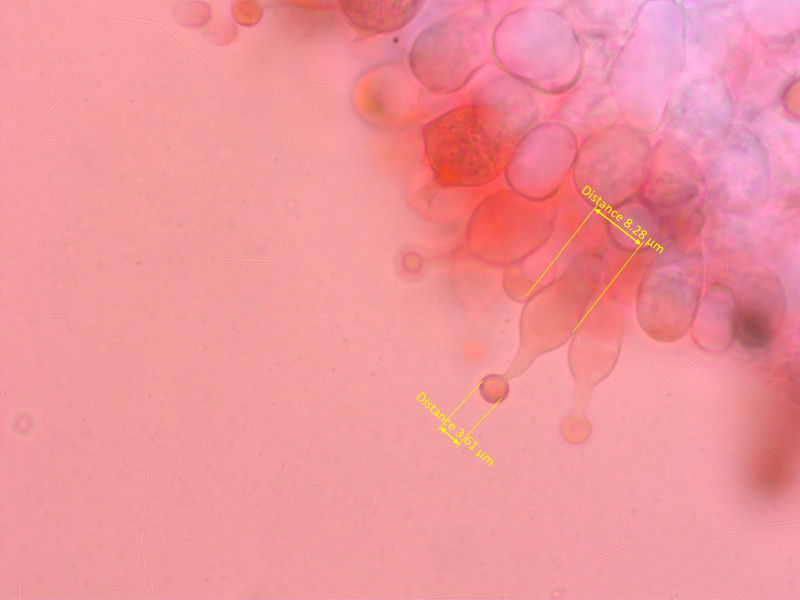
Cheilozystiden...
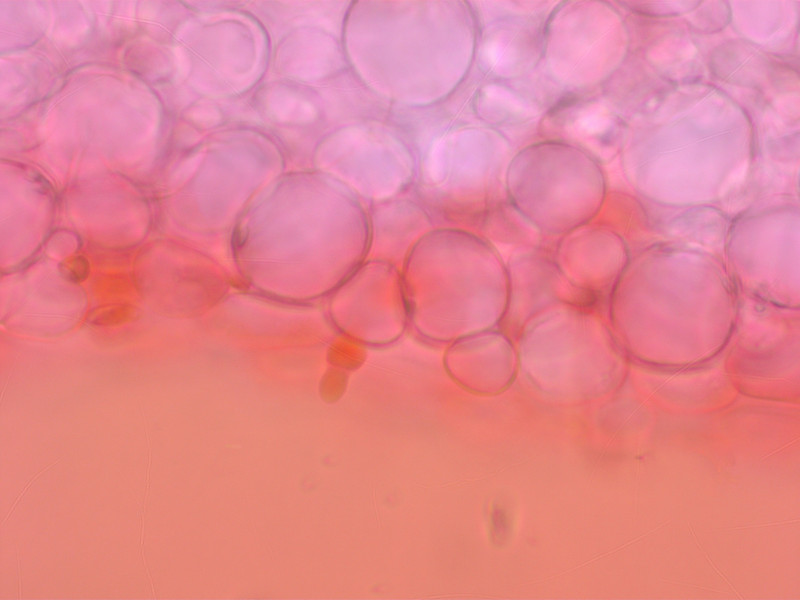
... HDS mit einzelnen Pileozystiden...
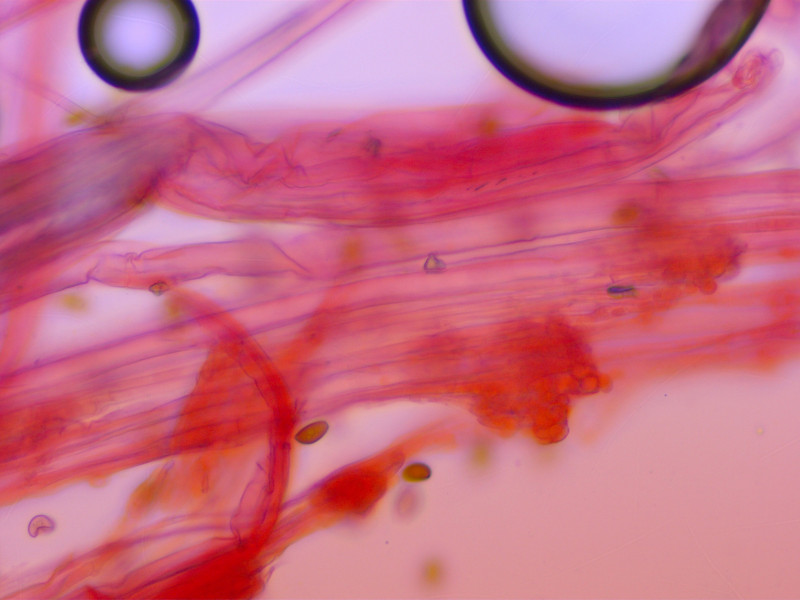
... und Stiel ohne lecythiforme Kaulozystiden.
[trennlinie][/trennlinie]
Und beim zweiten Samthäubchen kommt Freude auf:

2: Conocybe aurea - die vermehren sich wie die Karnickel.
Im Mai fand ich die ersten paar jämmerlichen Fruchtkörper, es kommen immer wieder neue und immer mehr.
Ich schätze jetzt die Population auf 40-50 Fruchtkörper. Sie sind mir höchst willkommen, ich würde wohl eher die Gemüseernte opfern als diese Pilze zu schädigen.
[trennlinie][/trennlinie]
Am Sonntag war ich noch kurz im Wald, da war wenig los, aber immerhin:

3: Mycena viridimarginata

Die grünen Schneiden kann man hier nur erahnen, mit einer starken Lupe sieht man sie am Hutrand recht gut.
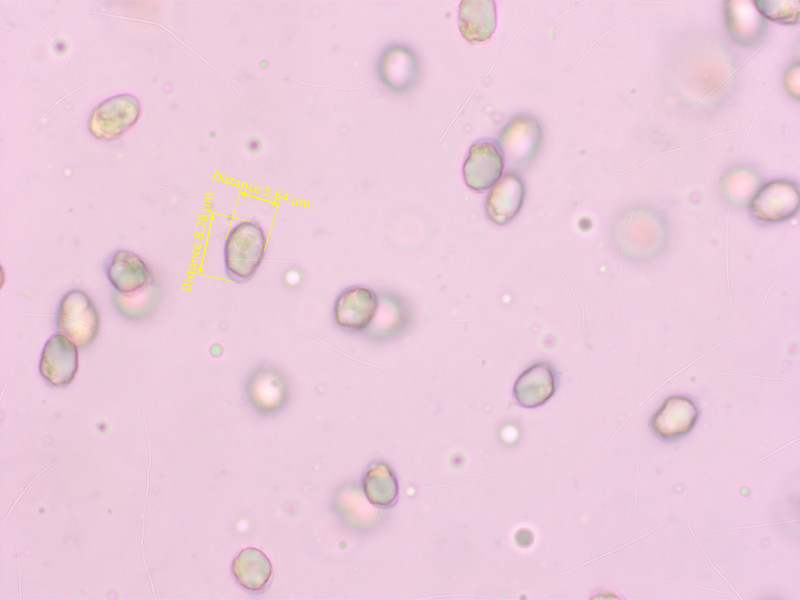
Sporen in Melzer
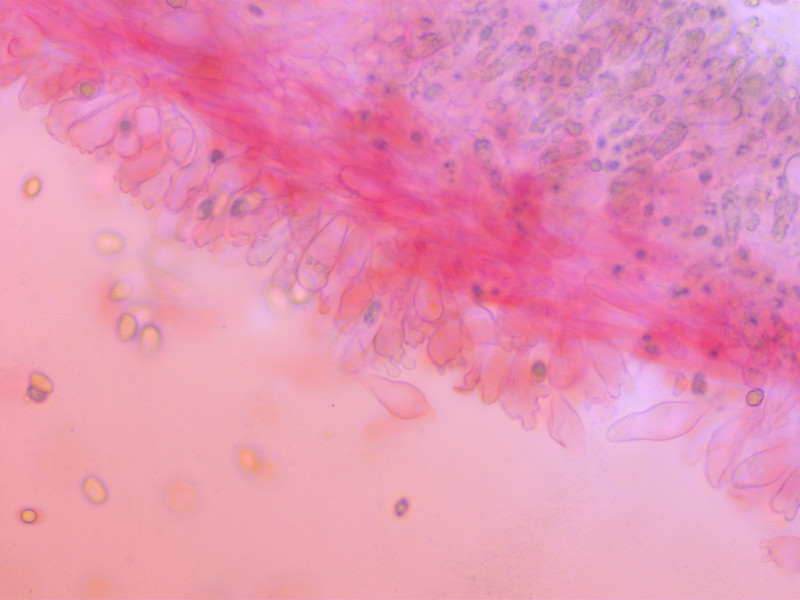
Cheilozystiden mit fingerförmigen Auswüchsen
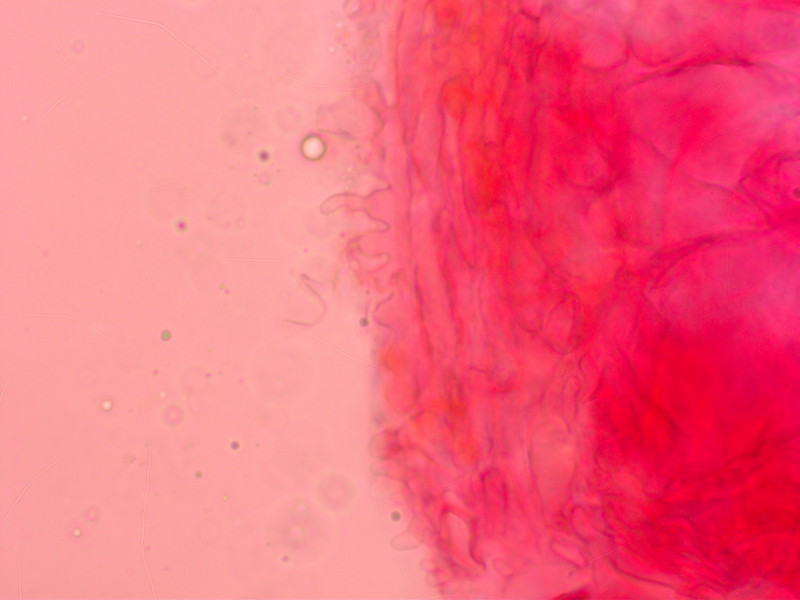
HDS mit kleinen Auswüchsen

Stipitipellis ebenso
[trennlinie][/trennlinie]
Und dann noch eine unerwartet schwierige Bestimmung. Ich hatte die nur aus Langeweile mitgenommen. Ein Purpurfilziger Holzritterling halt.
Aber eben nicht der Arttypus, sondern:

Tricholomopsis rutilans var. albofimbriata

Hier sieht man die Lamellen, die fast glasig wirken. Grund dafür:
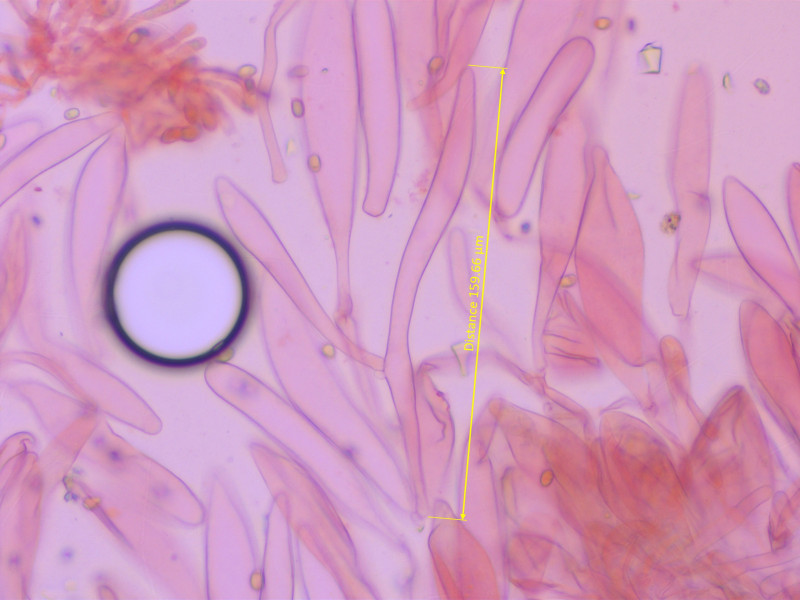
Riesige Cheilozystiden. Im Gegensatz zur normalen Tricholomopsis rutilans gibt es zwei auffallend verschiedene Formen von Zystiden:
Relativ kleine/keulige, und riesige, schlank spindelige. Letztere sind häufiger, kollabieren aber nach 2-3 Tagen im Kühlschrank zunehmend.
Die spindeligen Zystiden sind teilweise septiert oder gegabelt.
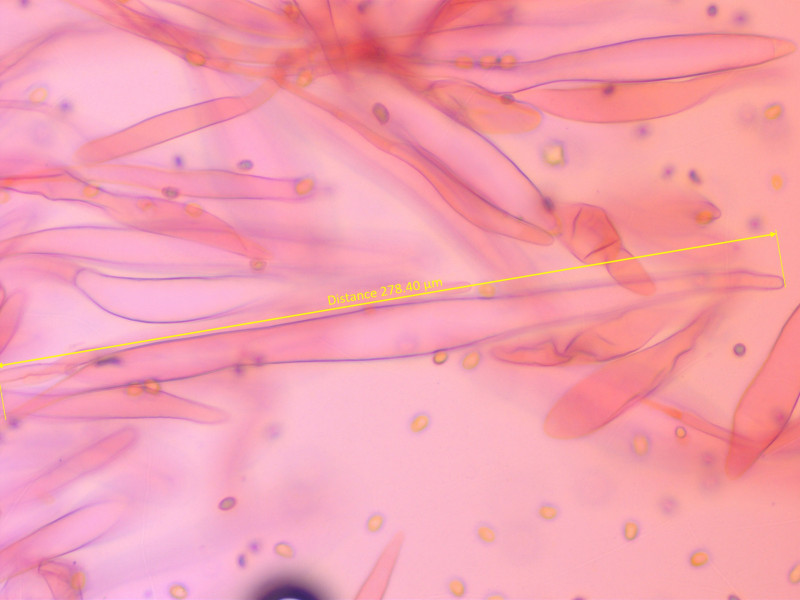
Ich konnte Zystiden bis fast 300 µm finden, damit übertreffen sie bei weitem alles was ich in der Literatur finden konnte (Maximum in der Funga Nordica mit 200 µm).
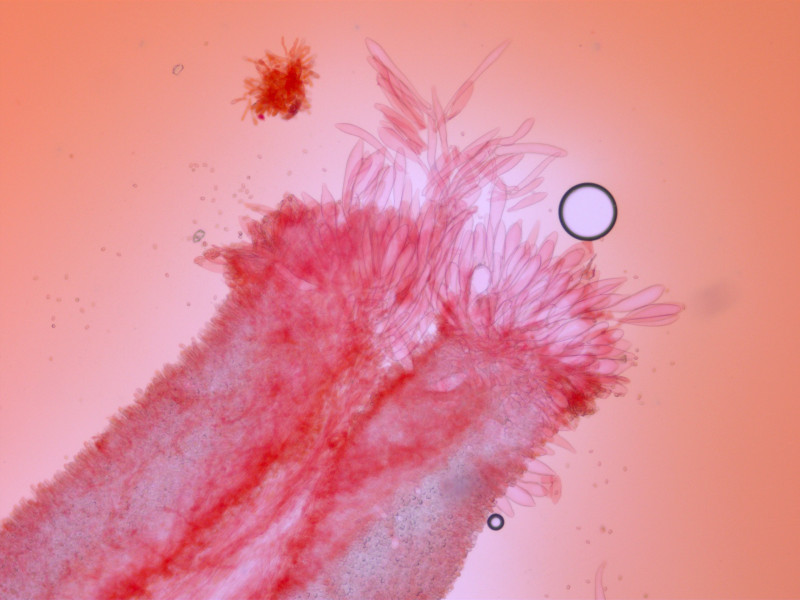
Pleurozystiden waren fast keine vorhanden, wenn überhaupt dann direkt bei der Schneide.
Dadurch scheidet die kleine Tr. flammula aus.
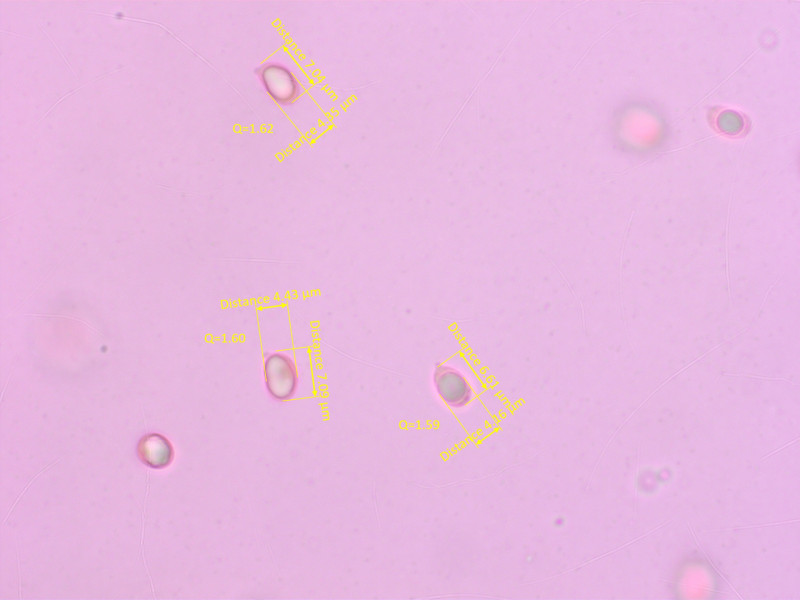
Die Sporen haben einen etwas höheren Q-Wert als beim Arttypus. Meistens um 1.6, einzelne bis 1.9.
Diese Varietät findet sich in der mir verfügbaren Literatur selten.
Die Darstellung in von A.H. Smith 1960 (Tricholomopsis (Agaricales) in the Western Hemisphere - Brittonia 12) überzeugt mich aber.
Ludwig erwähnt sie zwar, macht es sich aber zu einfach ("mit weisser Lamellenschneide"). Auf die doch deutlichen mikroskopischen Unterschiede geht er nicht ein.
Ob diese Varietät schon molekular untersucht wurde weiss ich nicht, mal abwarten.
In der Gattung werden ja laufend neue Arten beschrieben, es würde mich nicht wundern wenn diese Varietät irgendwann in den Artrang erhoben wird.
Lg, Raphael


