N'abend,
war vorhin mal kurz auf der Wiese schauen und war verblüfft, wie viele Rötlinge da jetzt stehen - mindestens 10 Arten - alle auch in ordentlichen Kollektionen. Allerdings hatte ich keinen Fotoapparat mit und die danach gemachten Bilder lassen sich nicht einlesen. Also nur ein paar Handybilder - 6 Arten von oben nach unten durchnummeriert

näher anschauen wollte ich mir vor allem den Gelben, zwecks Unterscheidung E. incana / E. verae (1) und den mit der bunten Lamellenschneide (3)


1) HDS im Auflicht


Lamelle im Auflicht
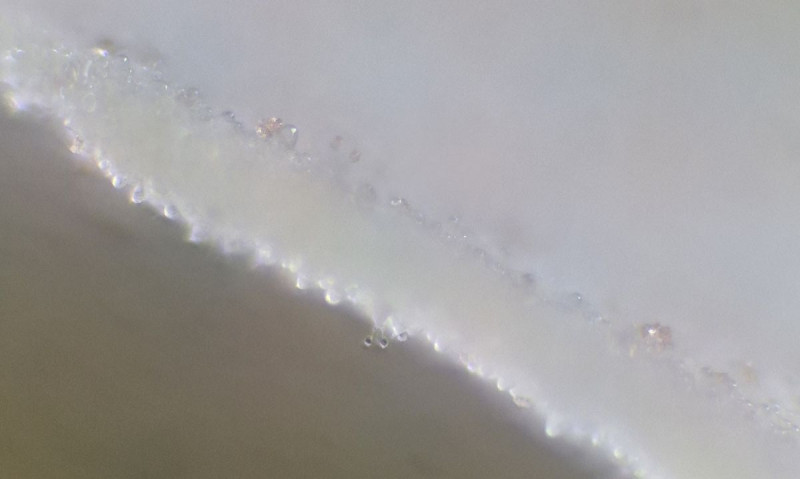
Durchlicht

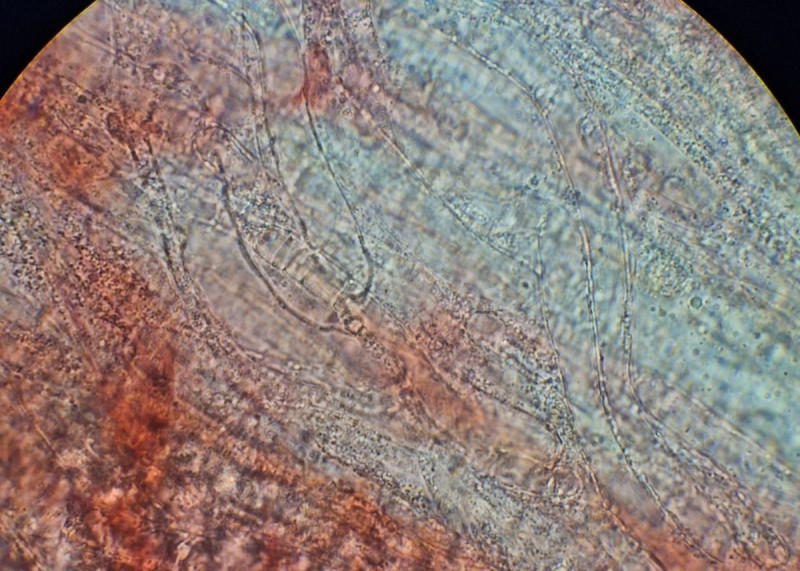
Übergang von HDS in Stiel

Basidien selten 4-sporig, vielfach 2-sporig und 3-sporig [das scheint es auch zu geben] -
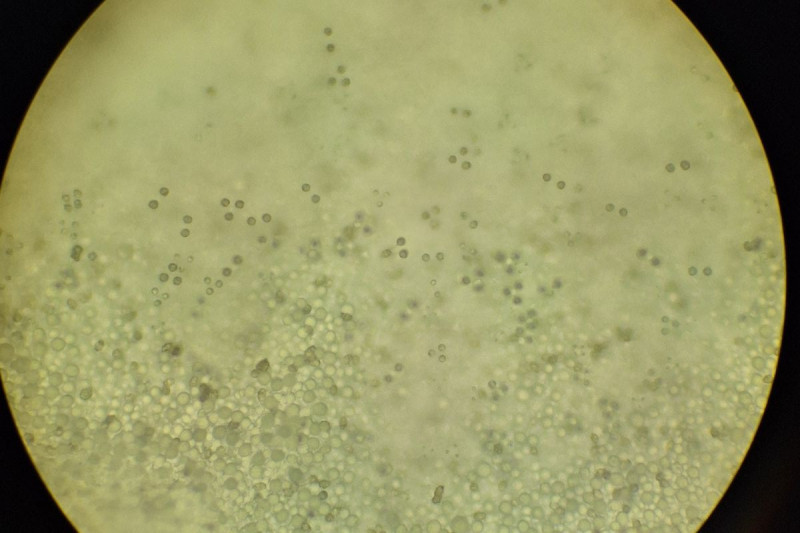
Lamelle in KR
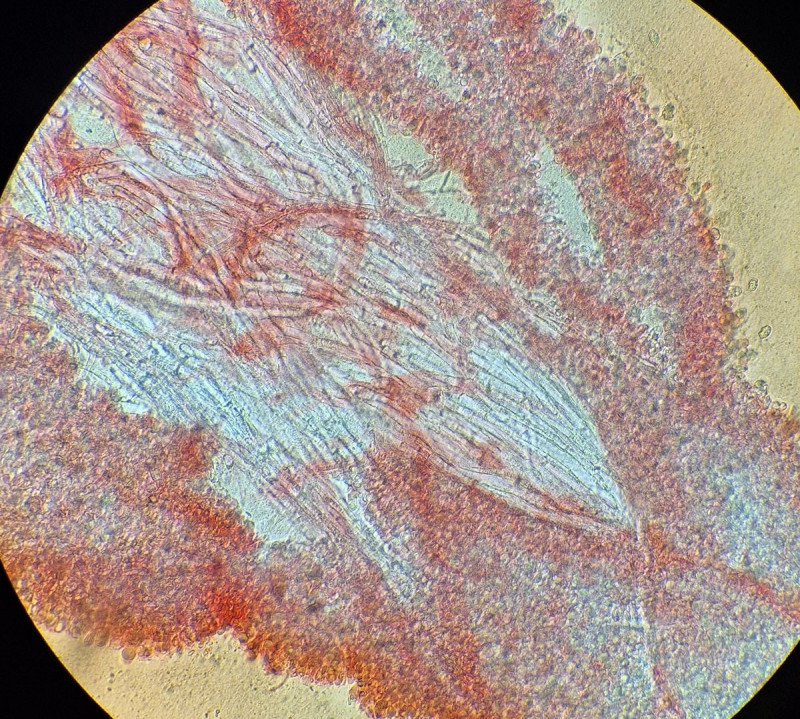
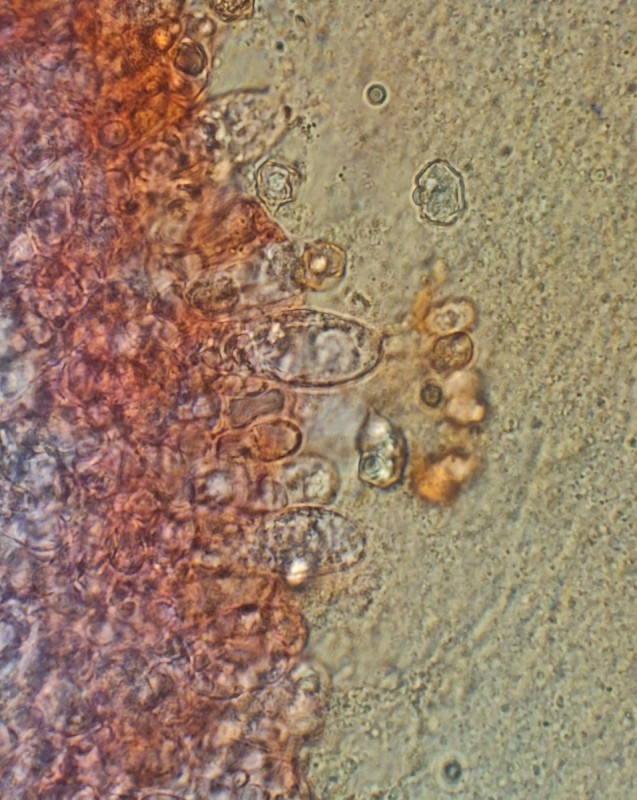
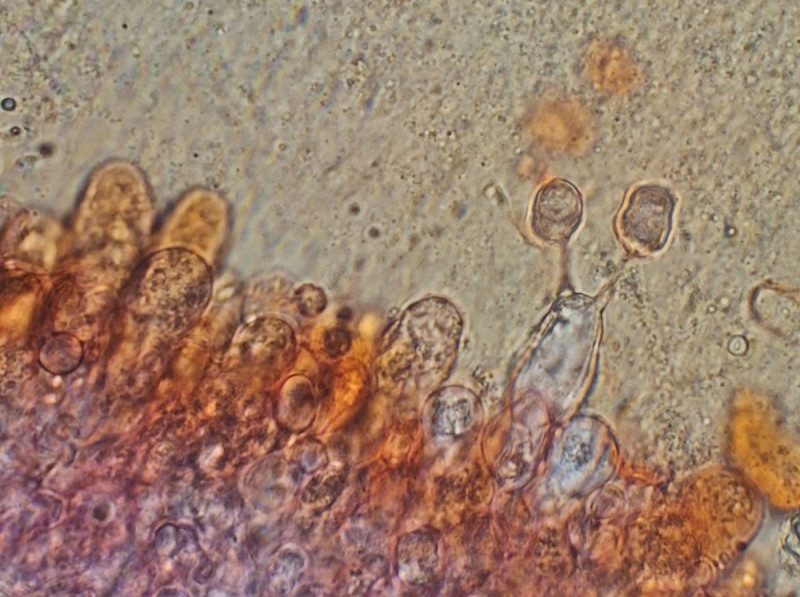
mittig spitze Elemente, Cheilozystiden?
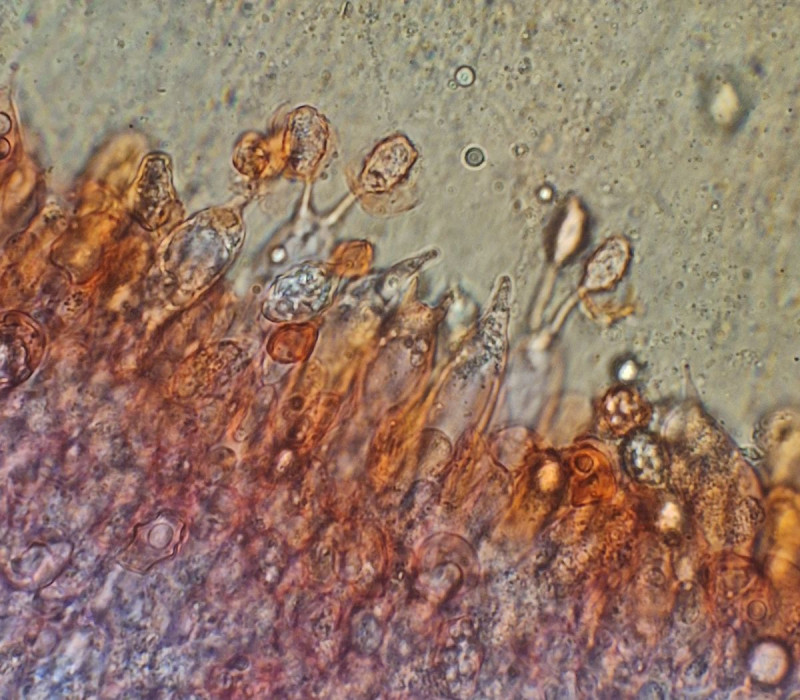
oder sind das Cheilozystiden?
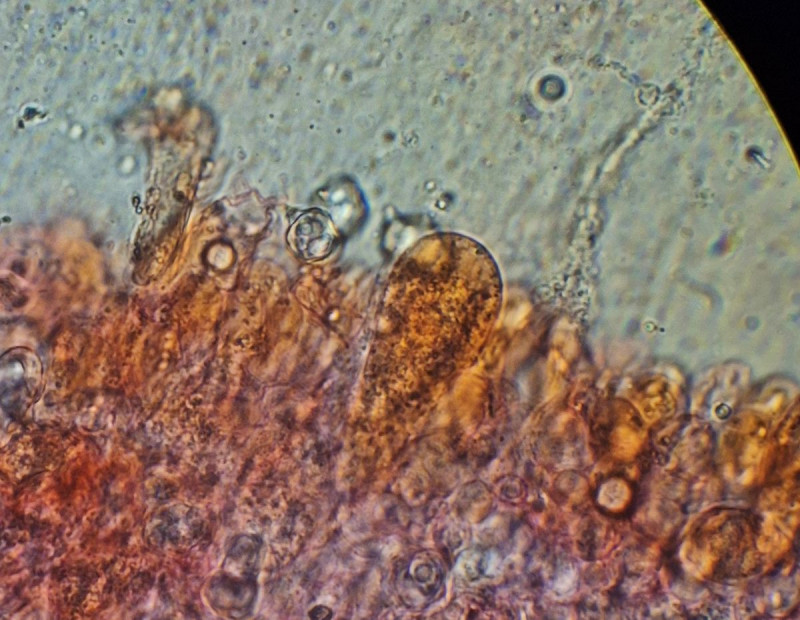
Sporen im Mittel 11,5*7,7, Q~1,5
Und welche Art ist das nun? In der Beschreibung heißt es:
"The second species is described here as new to science. Entoloma verae differs morphologically from typical E. incanum by the generally larger spores measuring 12.5 × 8 μm, on average, vs 10.5 × 7.5 μm on average in the neotype. But the size of spores can vary significantly, sometimes related to the presence of the 2-spored basidia."
Das interpretiere ich mal dahingehend, dass bei 2-sporigen Basidien größere Sporen ausgebildet werden. Dann stellt sich aber die Frage, wovon es abhängt, welche Basidien ausgebildet werden. Ist das Artspezifisch? Oder von Wachstumsbedingungen abhängig? Dann müsste man bei jeder Kollektion durchzählen, welche Basidien in welcher Menge vorhanden sind und die Größe der Sporen damit in Relation setzen. Bleibt dann der ohnehin geringe Unterschied der Sporengröße zur Arttrennung bestehen?
Fragen über Fragen. Aber da meine Exemplare ja ohnehin genau mittendrin liegen, bleibt es bei E. incana s. l.
2) zum Vergleich hier Nummer 2 mit 4-sporigen Basidien
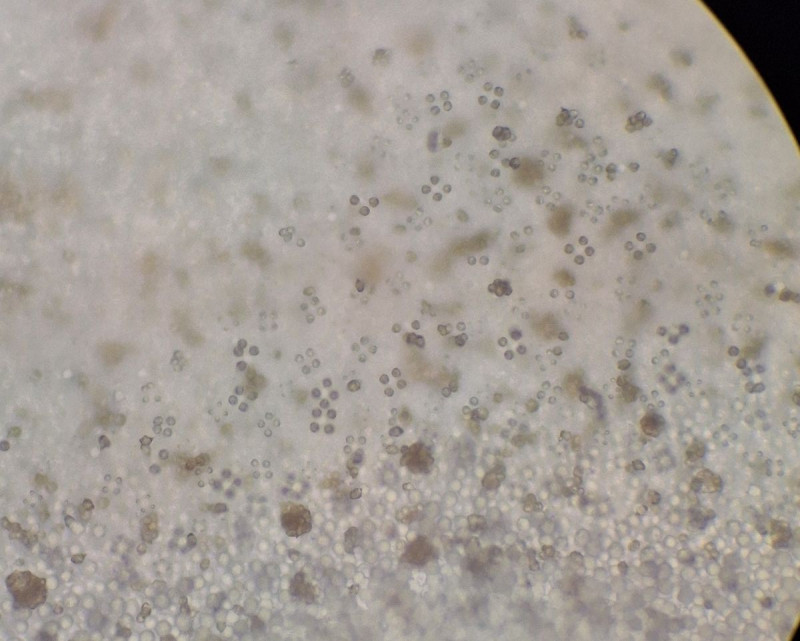
und mit reifen Sporenansammlungen, die die Lamellenkante rötlich färbt

3) hier sieht man schon, dass die Balufärbung nicht außen angelagert ist, sondern innen in der Lamellenkante



etwas tiefer fokussiert mit Basidien und Sporen
 ,
,
Durchlicht, auch hier 4-sporig
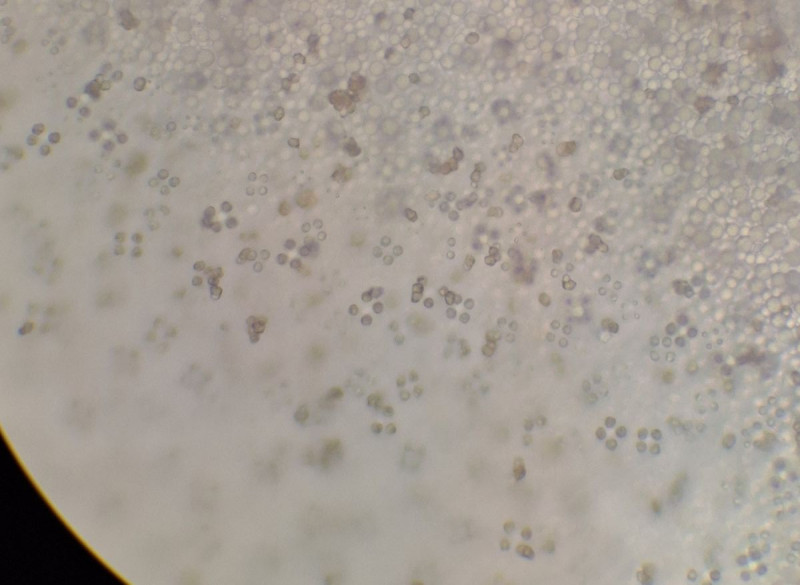
HDS in Wasser
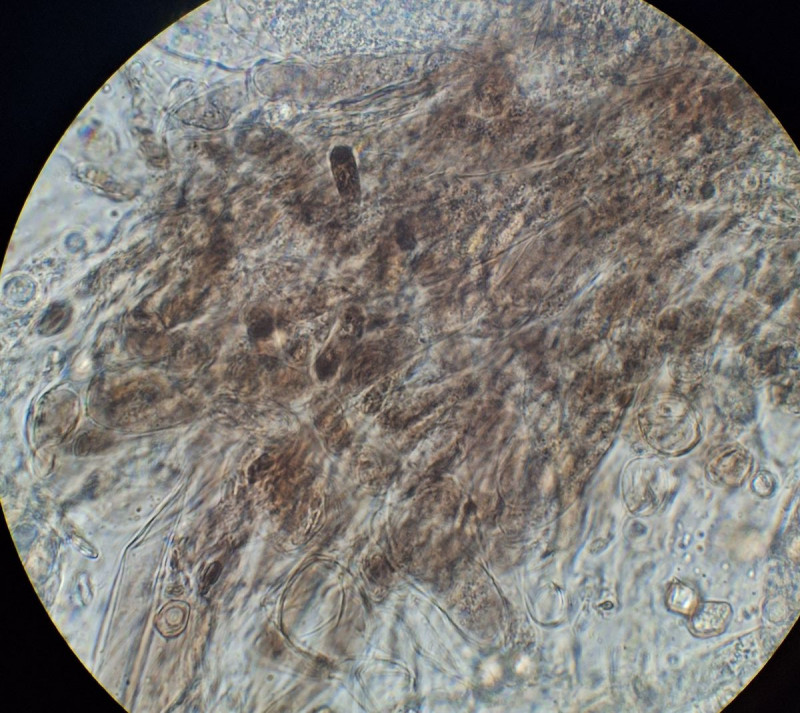
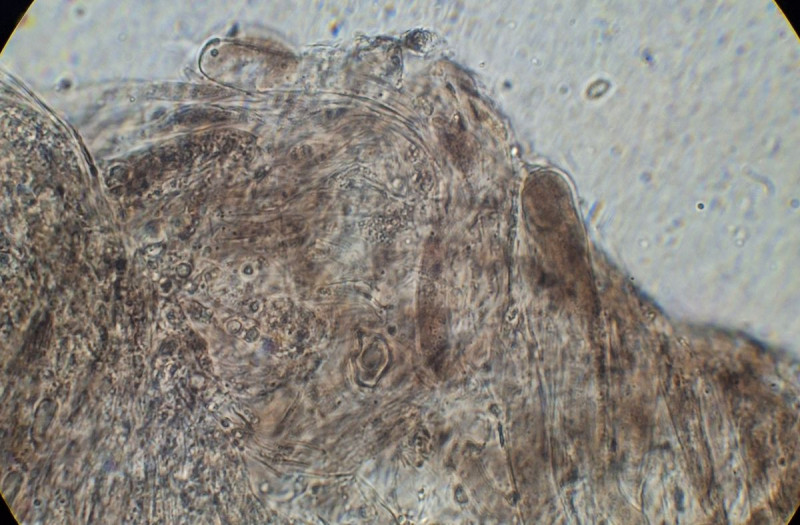
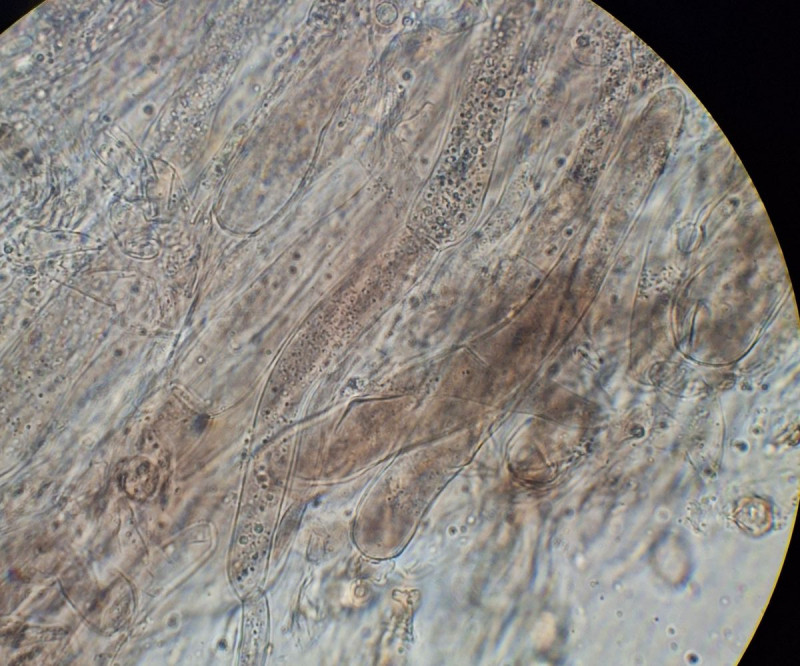
mit der baluen Lamellenschneide bin ich aber noch nicht zufrieden
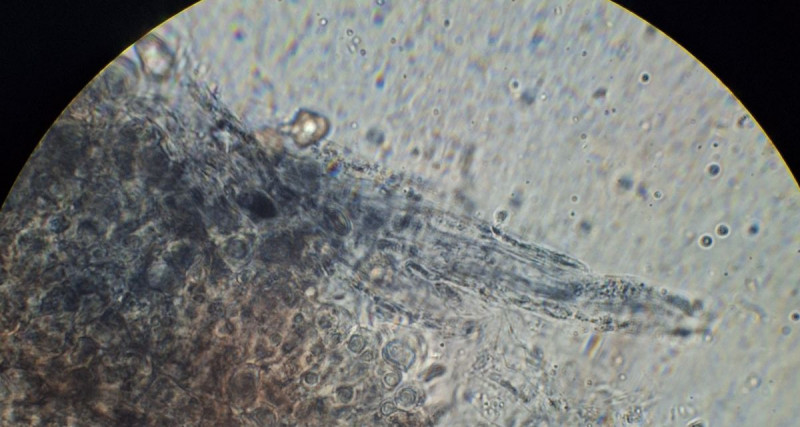
und in KR
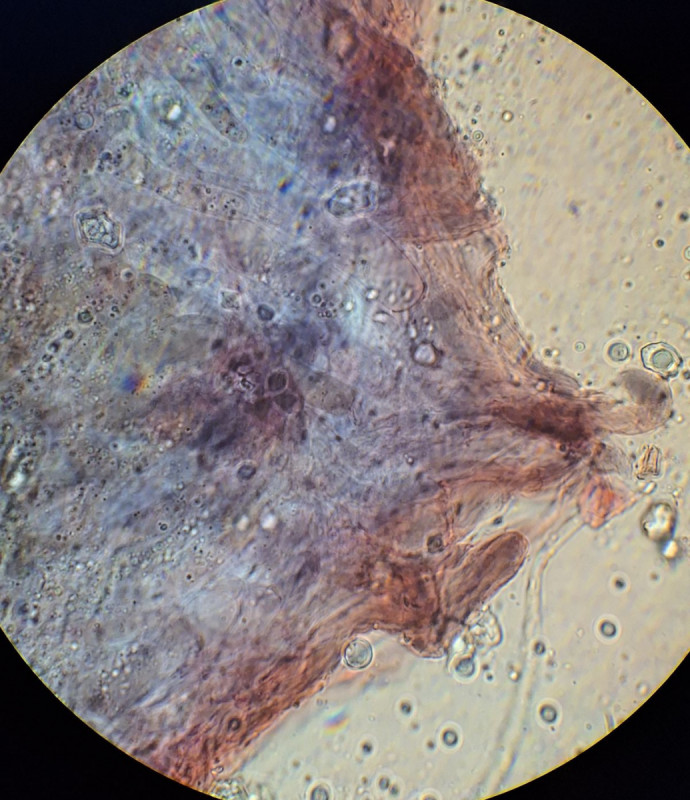
Sporen 9,7*7,7 Q~1,26
So, das war's. Danke für's Anschauen.
LG, Bernd


