Liebe Phytoparasitenfreunde,
bei einer Exkursion von letzter Woche konnte ich einen Fund, den ich heute mikroskopiert habe, partout nicht zuordnen. Zumindest bladmineerders.nl kennt hier keinen Pilz, zu dem die beobachteten Konidien passen. Aber zuerst einmal die makroskopische Beschreibung. Im Feld fielen mir auf Acer campestre folgende Blattflecken auf:


Unter dem Binokular konnte ich bis auf schwarze Verkrustungen, die ich mit bloßem Auge für Pyknidien gehalten hatte, zuerst nichts erkennen. Schließlich fielen mir bei 80facher Vergrößerung (vgl. Bild) auf der Blattoberseite kleine, Trichom-ähnliche, büschelig wachsende weiße Härchen im dunklen Randbereich der Blattflecken auf. Konnte es sich vielleicht um Konidienträger handeln? Tatsächlich konnten relativ schnell Trichome ausgeschlossen werden, da sich nach weiterer Suche "echte" Trichome wesentlich länger und einzelstehend oder nur direkt auf der Blattnervatur zu finden waren.



Bei epiphyllen Konidiophoren spare ich mir gerne das frimelige Herumschnippeln und bediene mich meines guten alten Freundes, des Tesafilmpräparats. Einfacher geht es nicht, einfach draufdatschen, abziehen, und man spart auch noch ein Deckgläschen ein. Tatsächlich waren die entsprechenden "Härchen"-Konidiophoren sehr gut unter dem Mikroskop einsichtbar, auch Konidien gab es en masse zu sehen. Hier ein paar Bilder in 400-facher Vergrößerung:
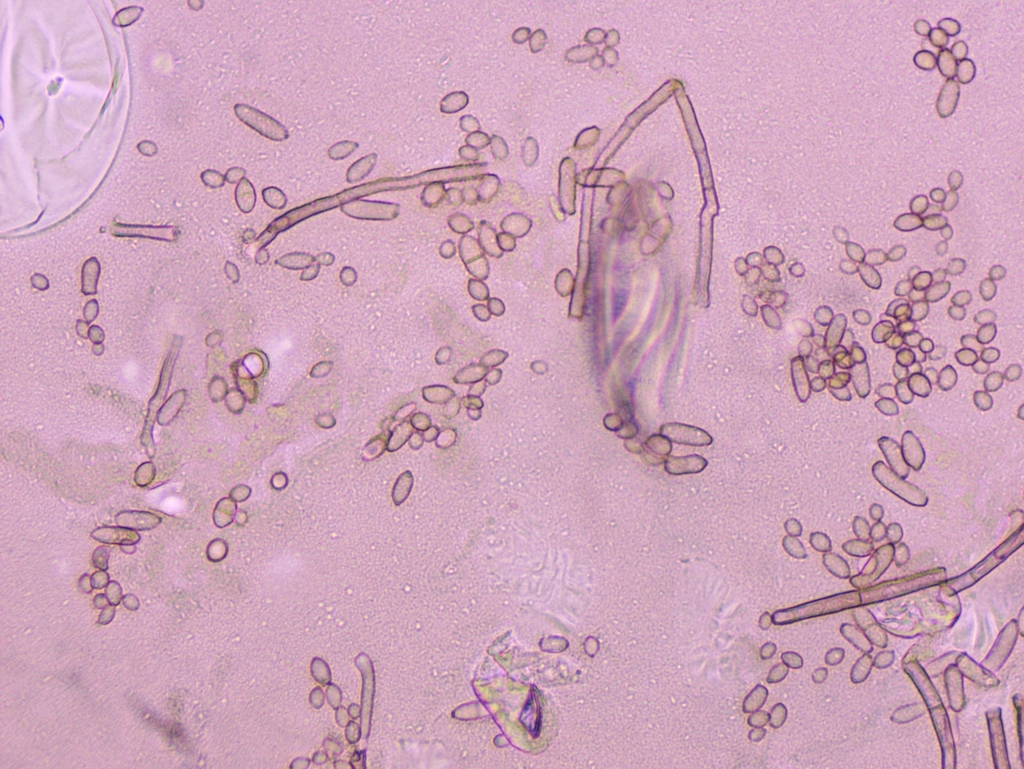
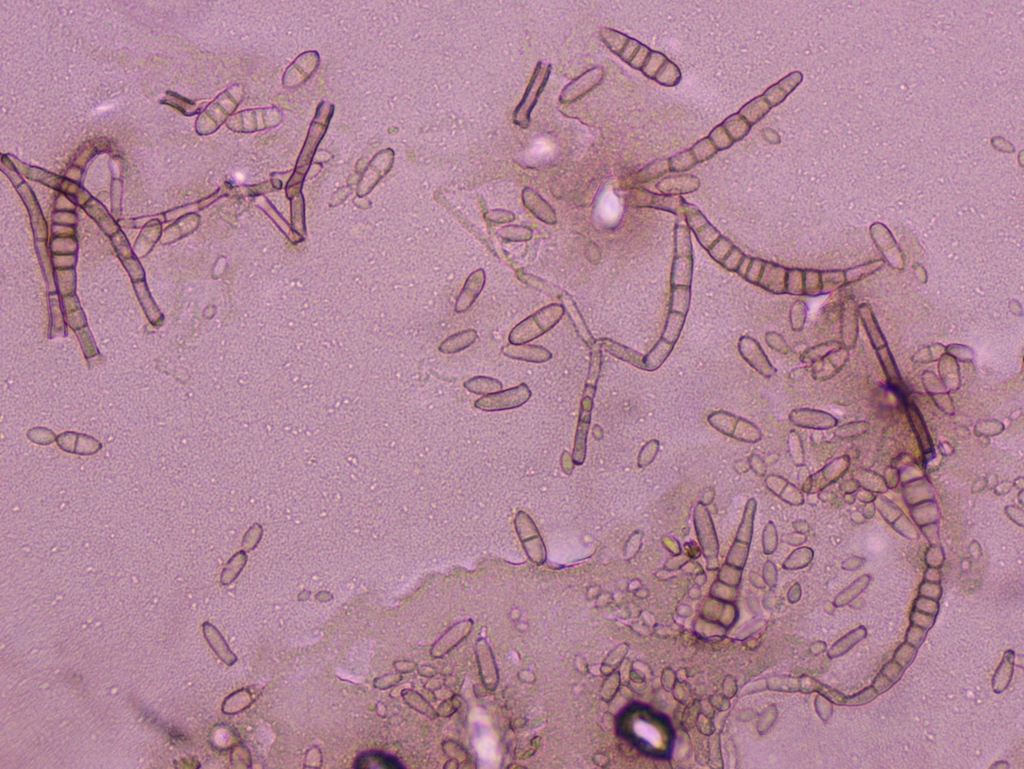
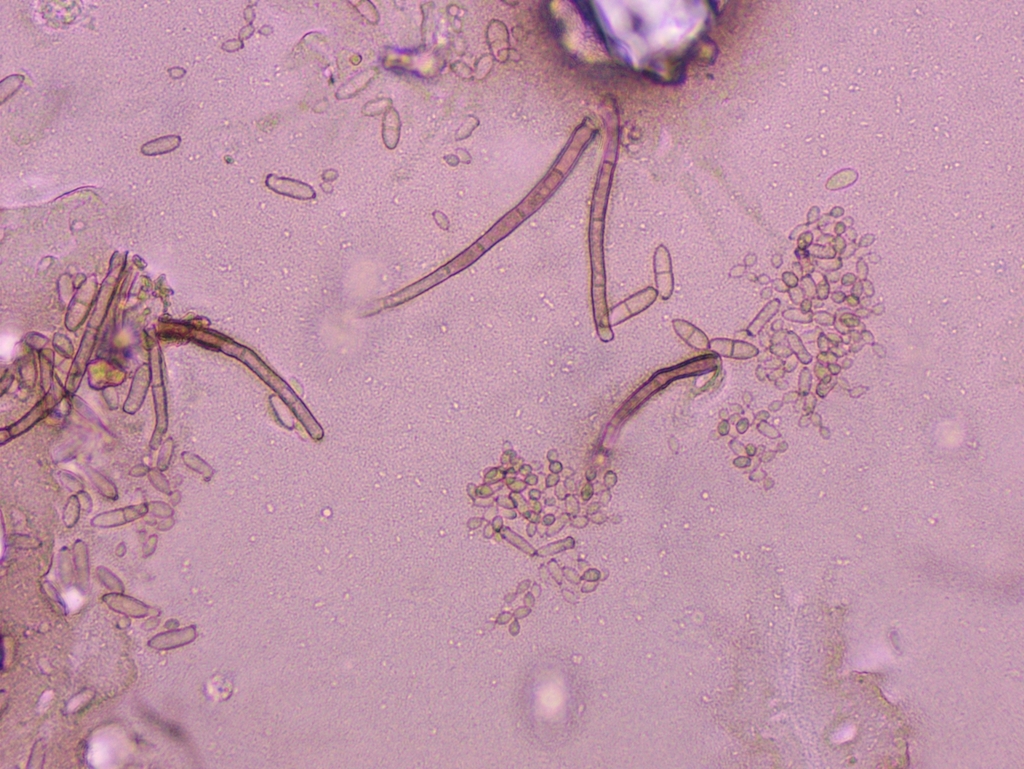
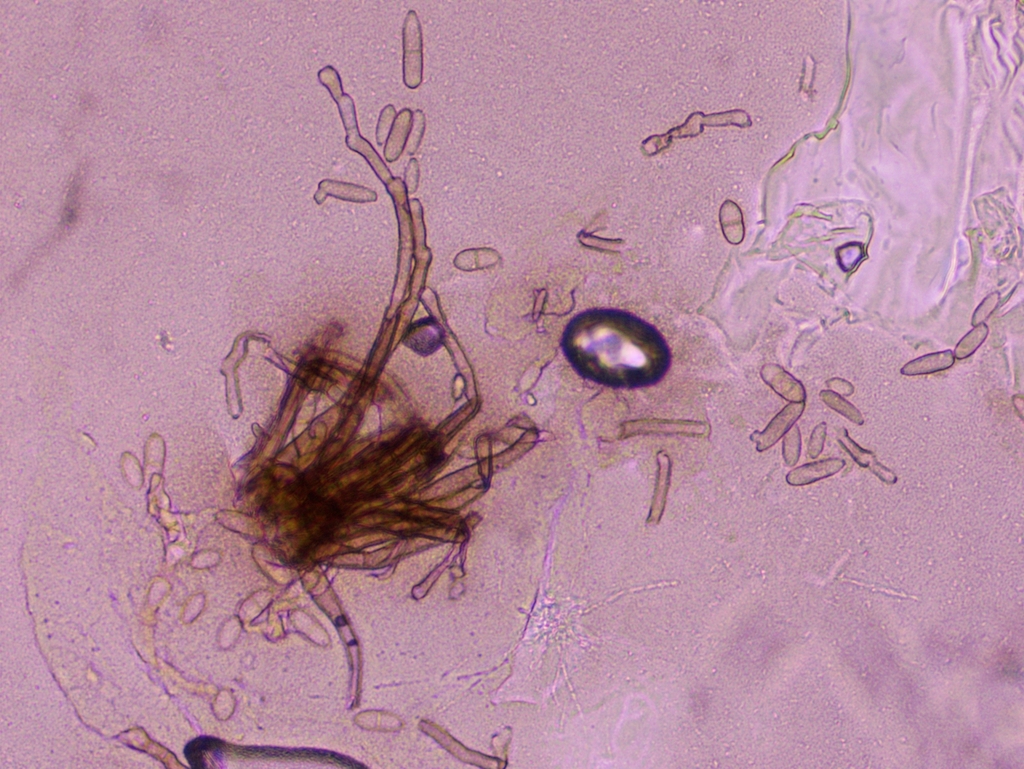
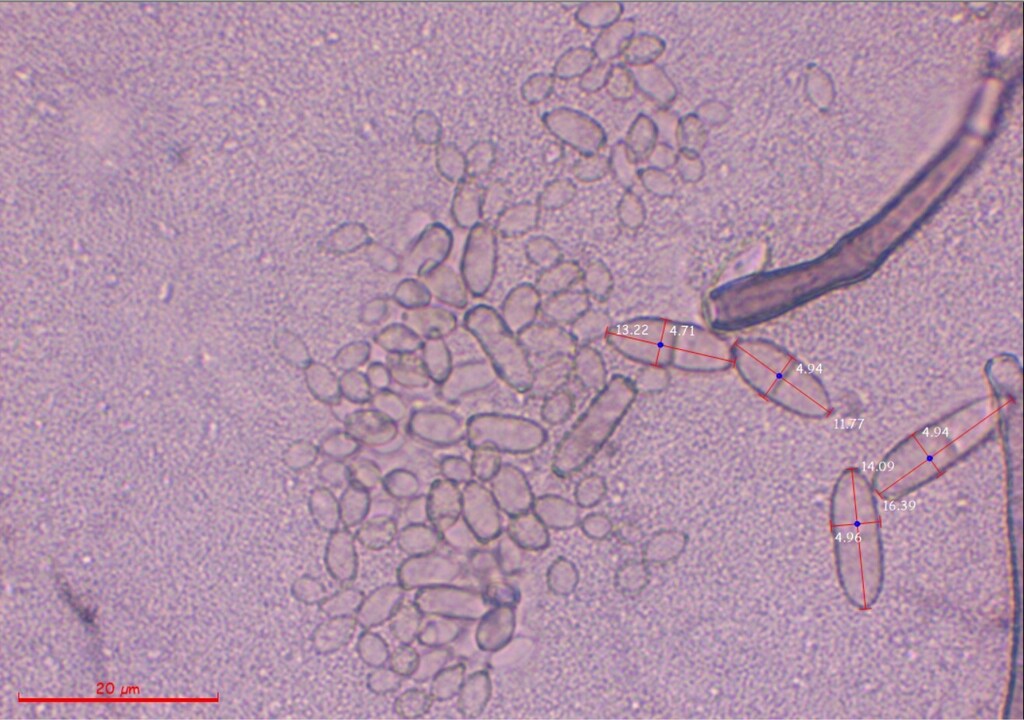
Es scheint mir hier ein Mischbefall von mindestens zwei, wenn nicht gar drei Arten vorzuliegen. Nun bin ich in die Ölimmersion gegangen und habe die unseptierten bis einmal septierten, eiförmig bis ovalen und manchmal leicht keulenförmigen Sporen ausgemessen, die wie auf dem Bild direkt über diesem Text definitiv direkt von den oben bereits beschriebenen büscheligen Konidiophoren ausgehen. Die großen, vielzelligen, sichelförmig bis keuligen Dictyosporen einerseits und die kleinen, rund-eiförmigen Sporen mit einer basalen, an ein Hilum erinnernden Narbe ignoriere ich bei der Messung.
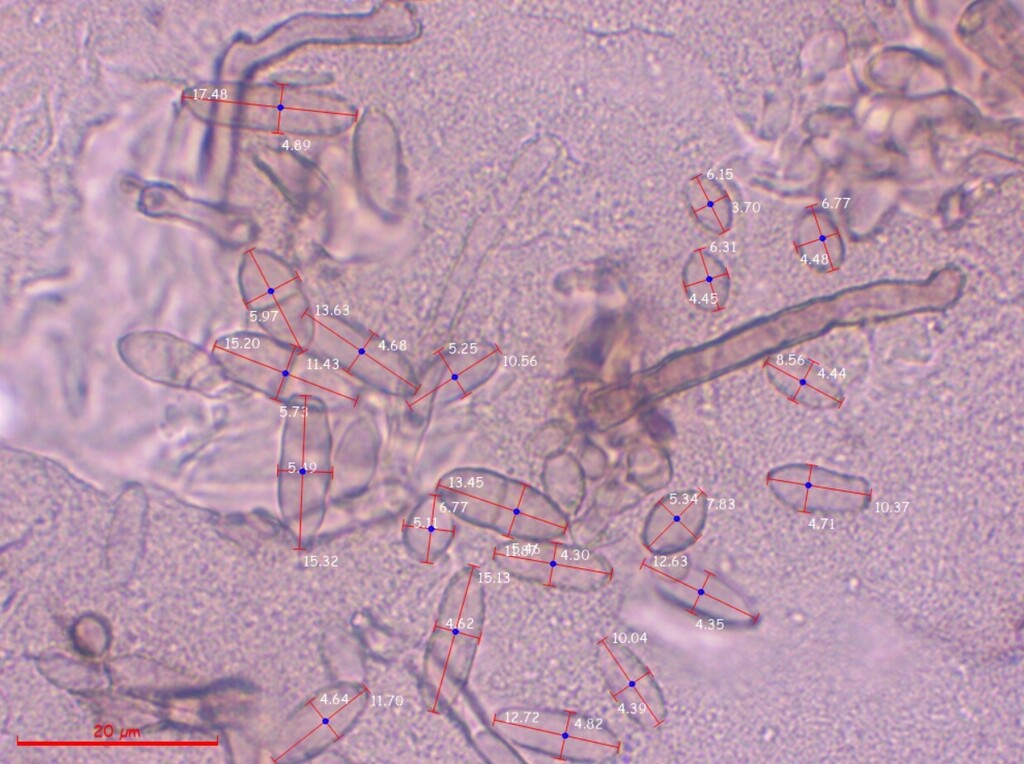
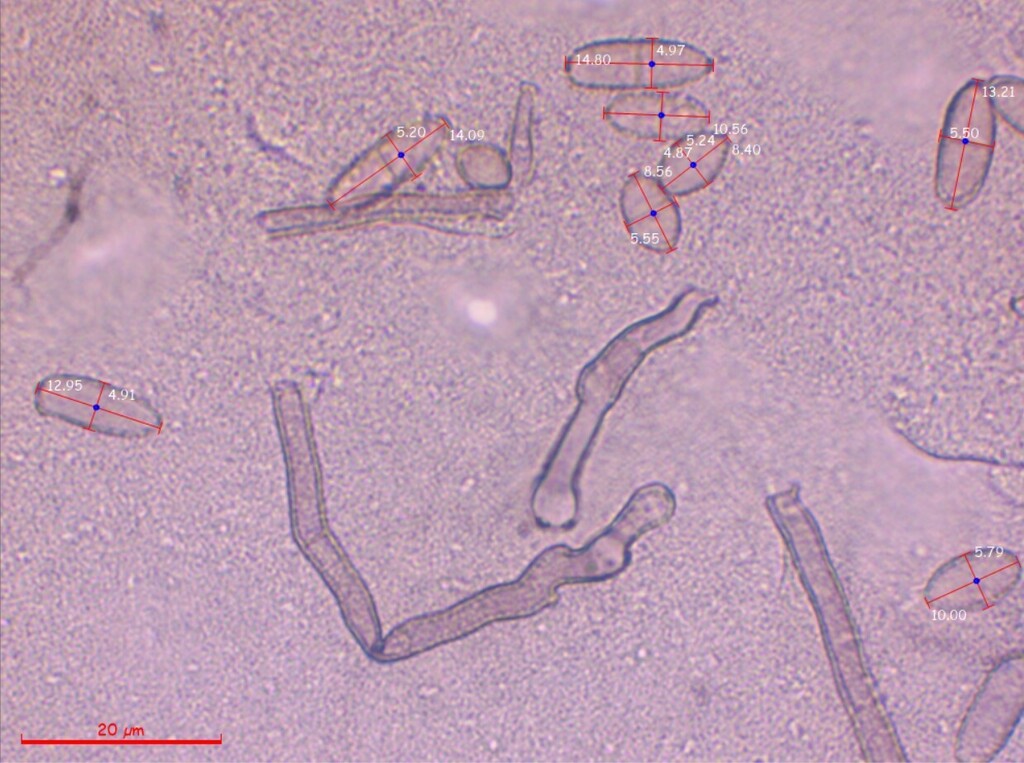
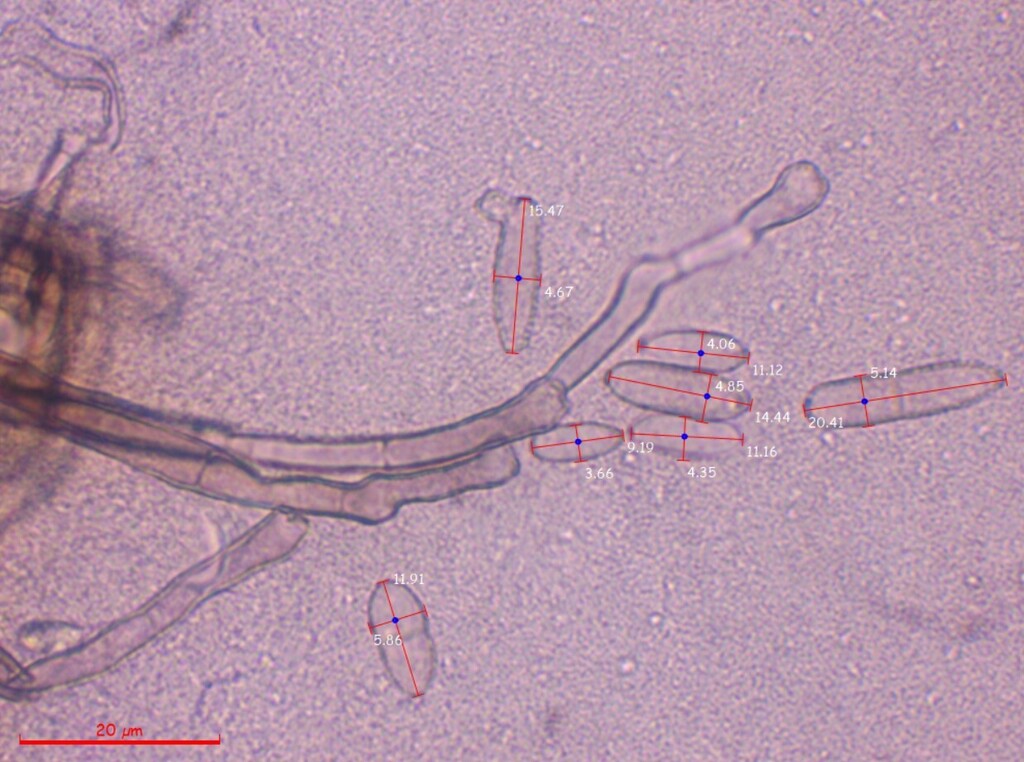
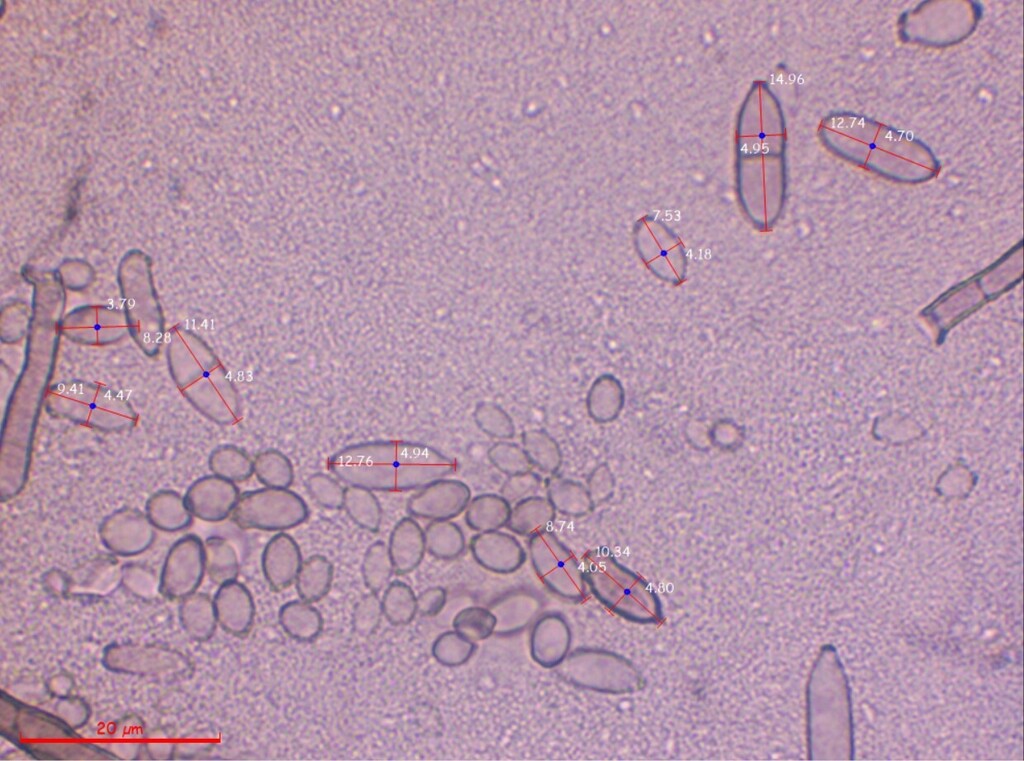
Auch wenn ich sie ignoriere, habe ich dennoch vor allem von den Dictyosporen ein paar Fotos gemacht:
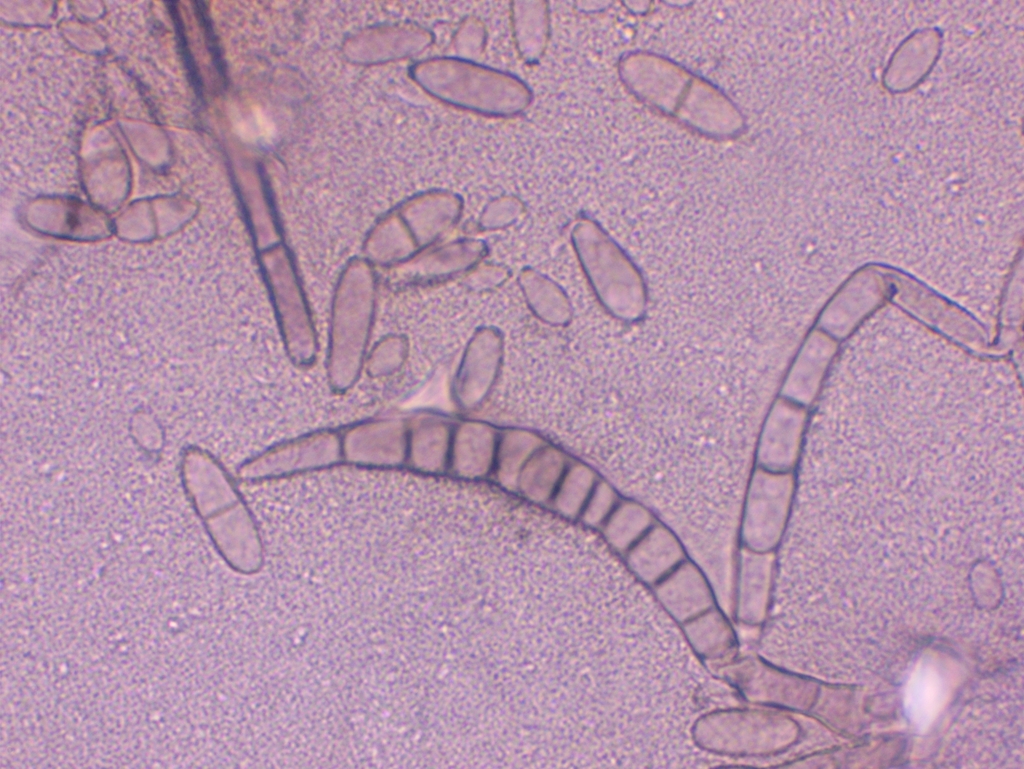
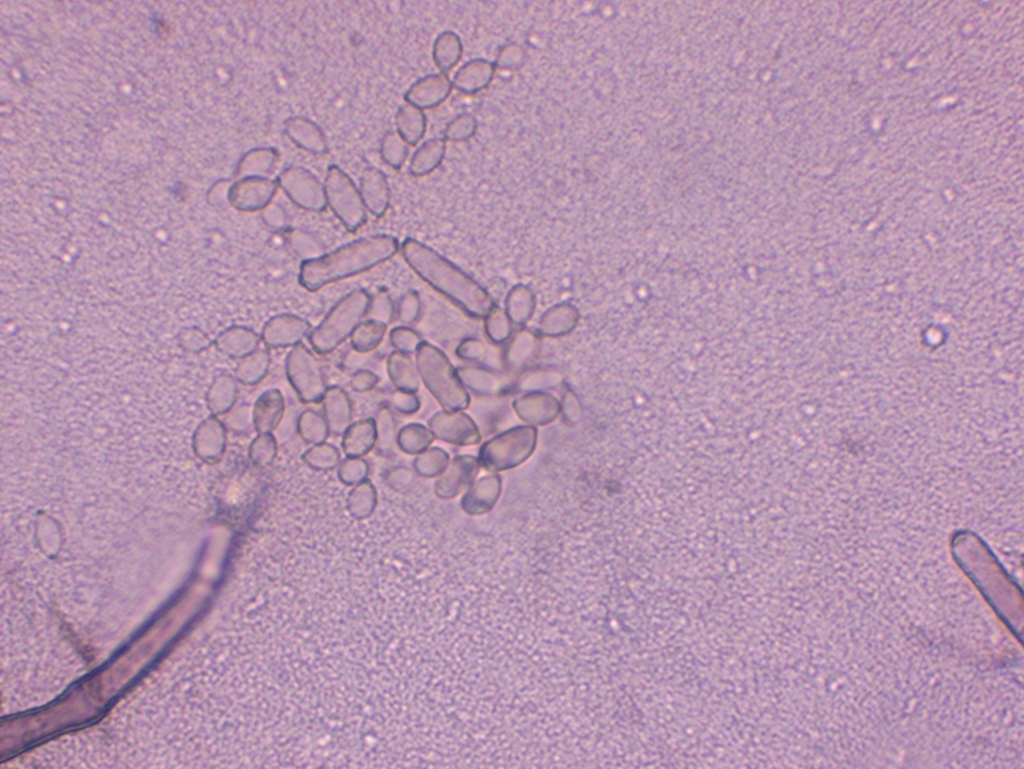
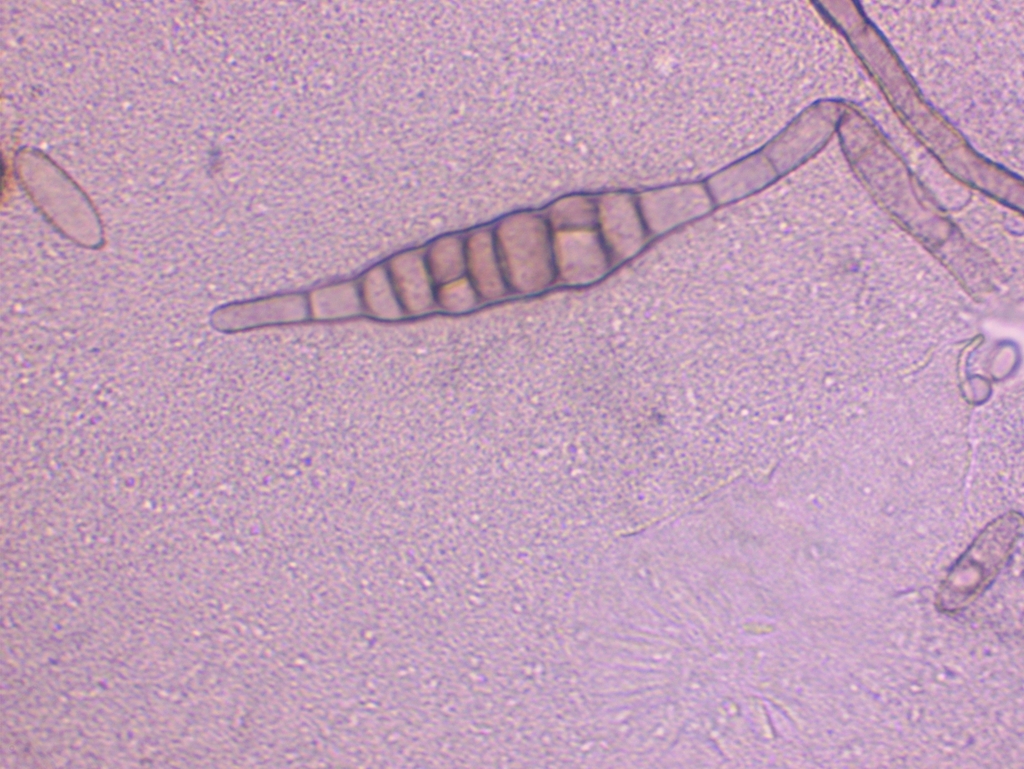
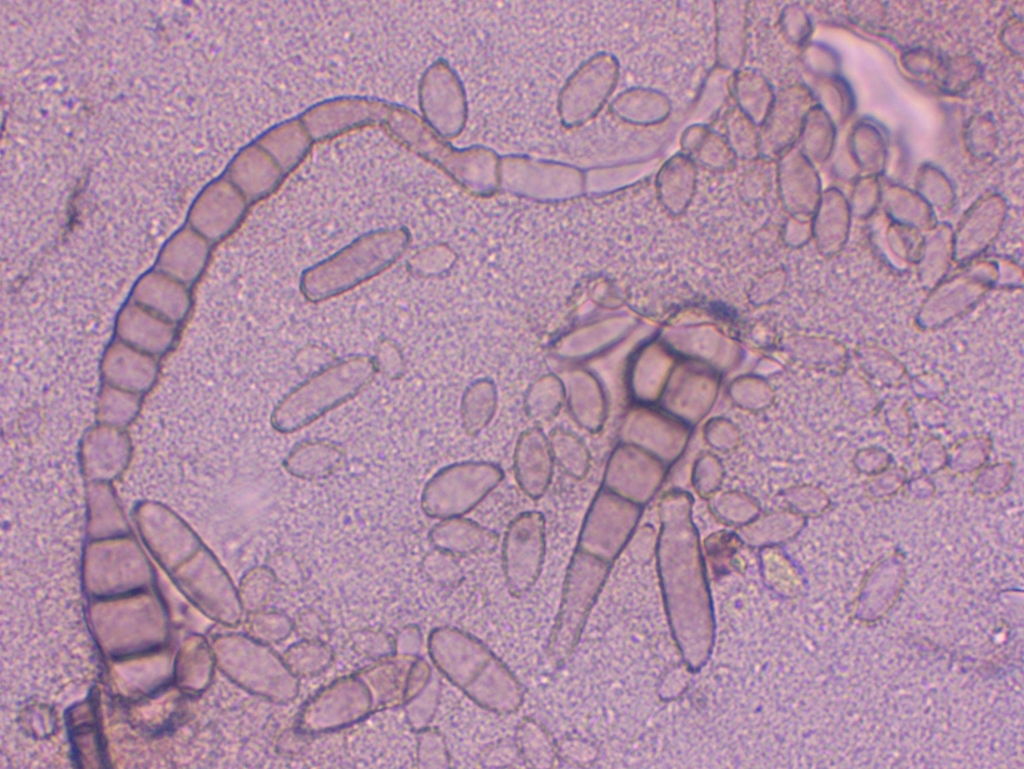
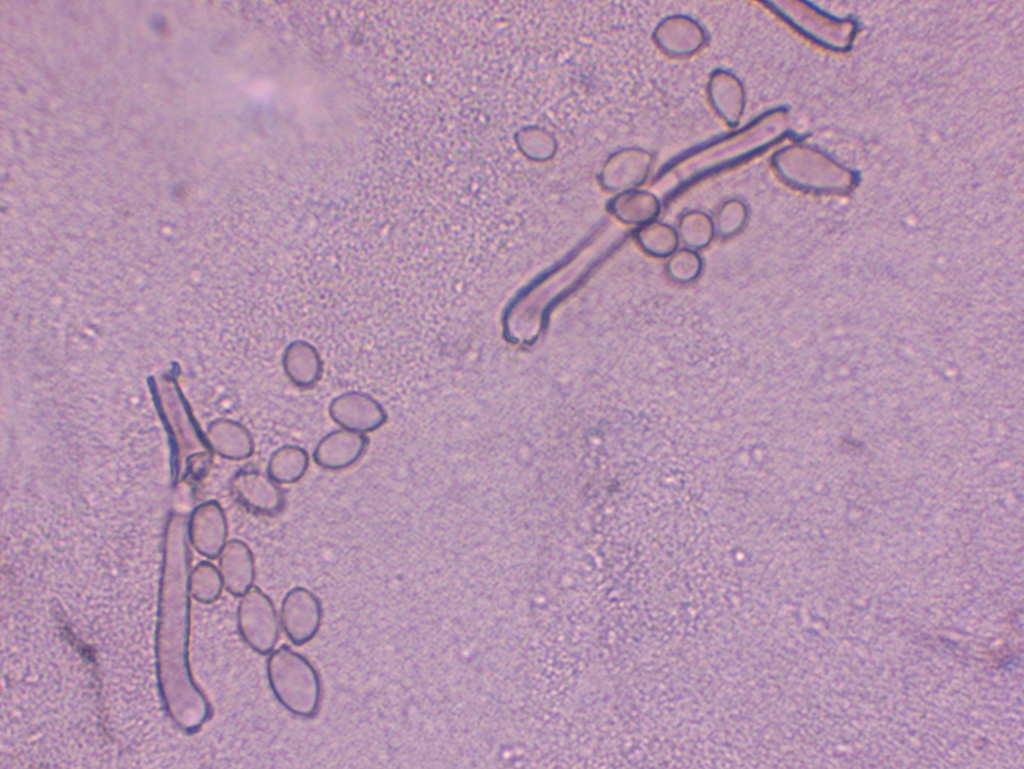
Nun noch die Auswertung der Messdaten:
(6.2) 7.8 - 15.2 (20.4) × (3.7) 4.2 - 5.5 (6) µm
Q = (1.3) 1.6 - 3 (4) ; N = 48
Me = 11.7 × 4.8 µm ; Qe = 2.4
Kann mir irgendjemand bei der Bestimmung weiterhelfen? Material ist noch vorhanden.
Beste Grüße, pedro.


