Hallo zusammen
An der Tagung unserer Wissenschaftlichen Kommission gab es einige sehr spannende Sachen.
Tag 1: Auf dem Weg zur Tagung in einem Auwald am Genfersee.
1:

Nicht unbedingt mein Ding, aber einfach bestimmbar: Multiclavula mucida.
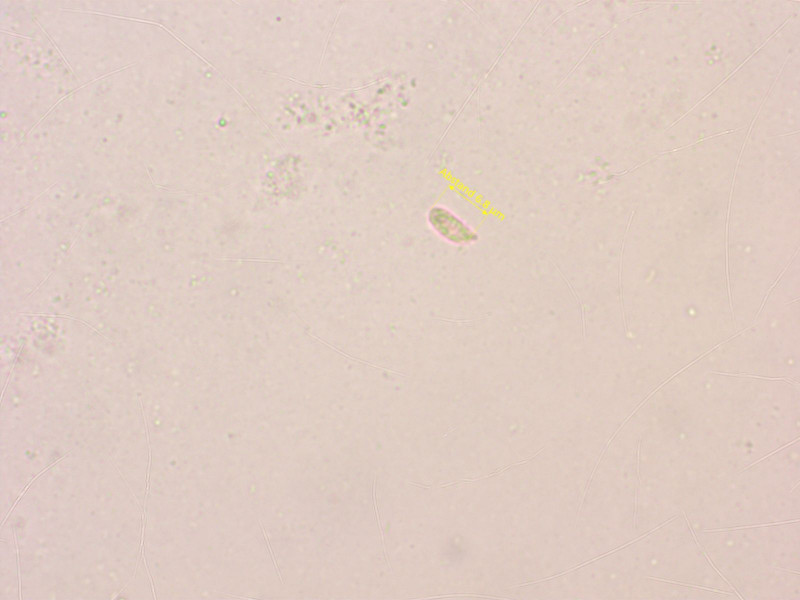
Sporen waren schwer zu finden.
2:

Ein Dachpilz auf einem liegenden Stamm (Pappel?): Pluteus cinereofuscus.
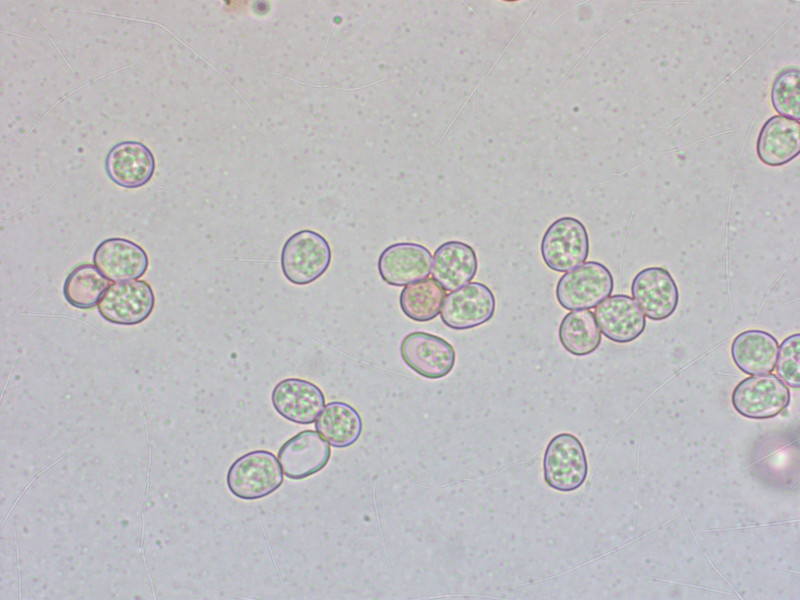
Dachpilztypische Sporen.
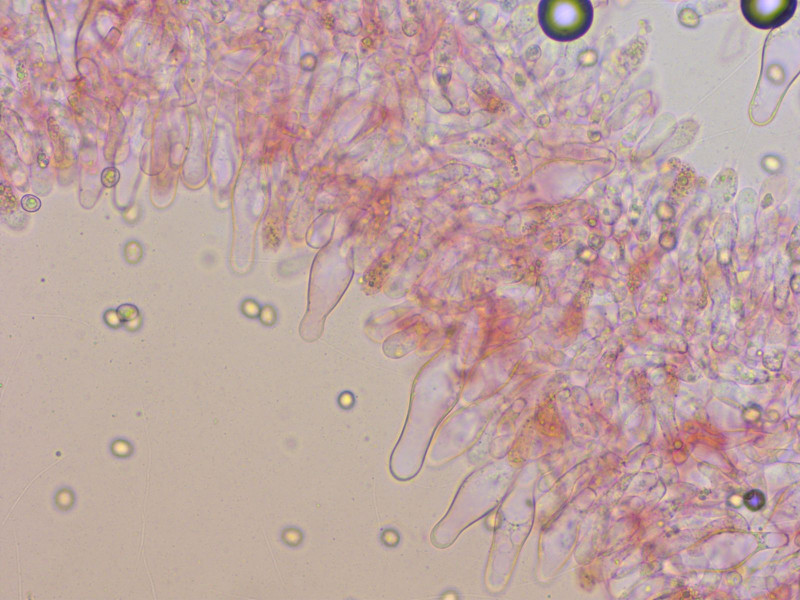
Cheilozystiden
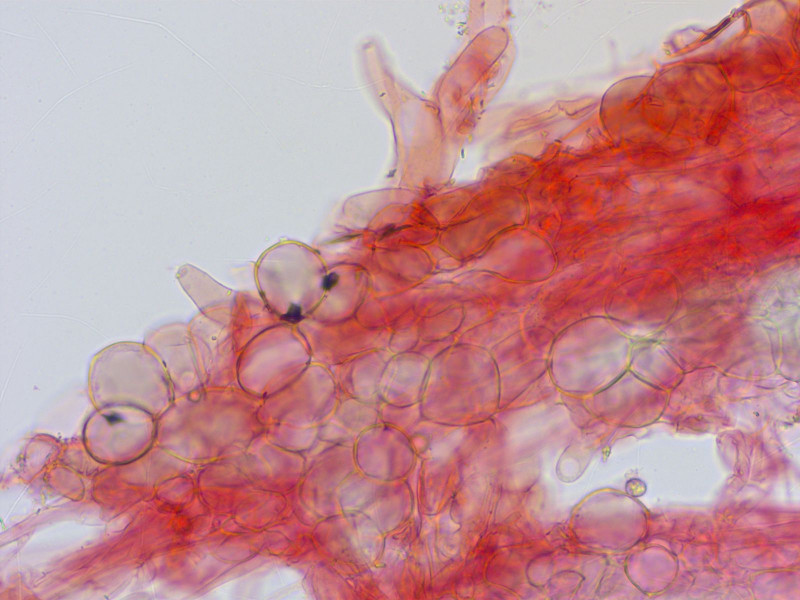
HDS hymeniform.
Tag 2: In einem Buchenwald
3:

Myochromella boudieri, typisch dieser dunkle Stiel mit hellen Fasern.
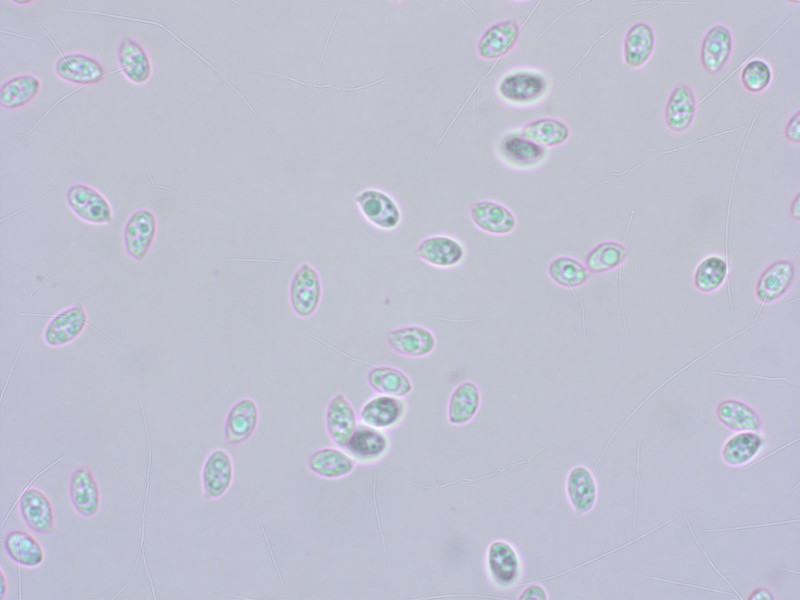
Sporen wenig aussagekräftig.
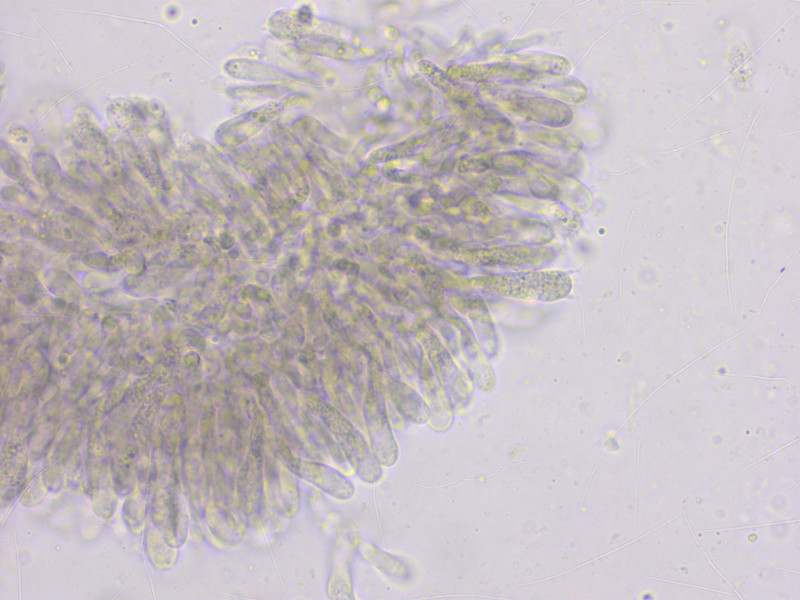
Basidien siderophil.
4:

Tricholomopsis sulfureoides wurde am gleichen Tag von drei verschiedenen Teilnehmern gefunden, offenbar doch nicht so selten.
Tag 3: Auf einer Saftlingswiese, wo es leider kaum Saftlinge gab.
5:

DIeser kleine Rötling mit konischem Hut und Papille lässt sich schon im Feld (mit Unsicherheit) ansprechen: Entoloma cuspidiferum.
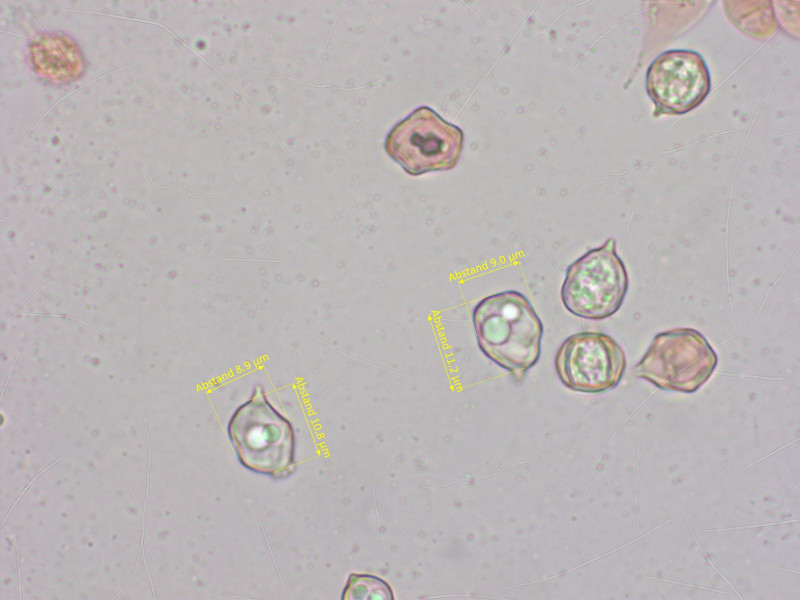
Sporen nur mit angedeuteten Ecken
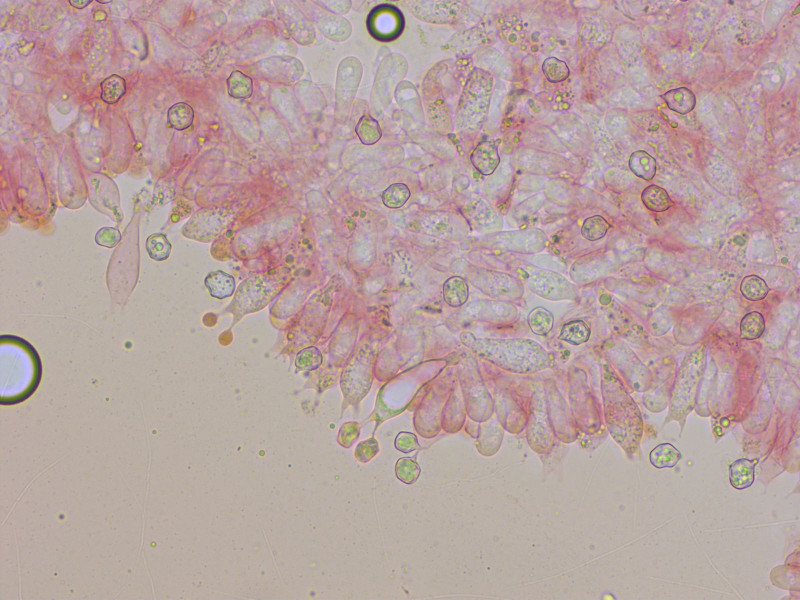
Basidien 2- oder 1-sporig
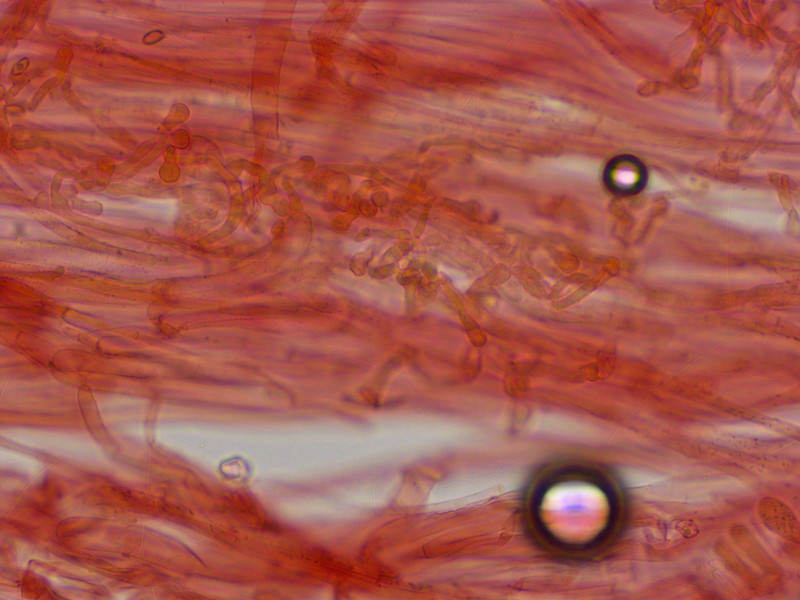
Typisch kopfige Kaulozystiden.
6:

Ein kleiner Häubling auf Holz. An dem dunklen Stiel und der Papille erkennt man ihn sogar makroskopisch: Galerina triscopa.
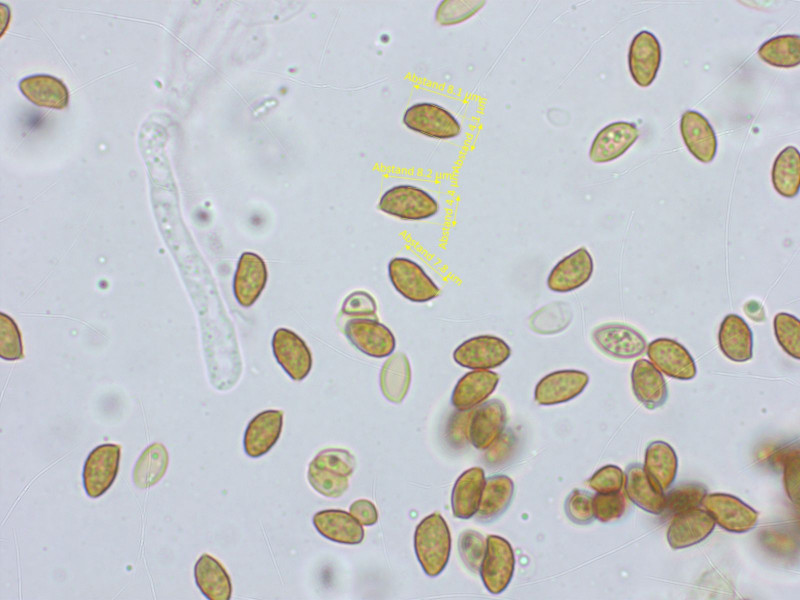
Sporen klein für die Gattung.
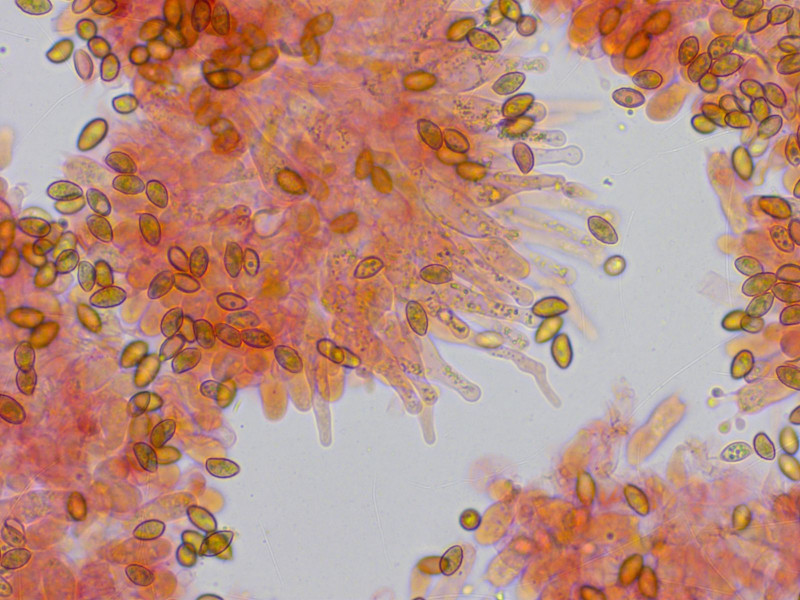
Zystiden zylindrisch oder etwas lageniform-bauchig.
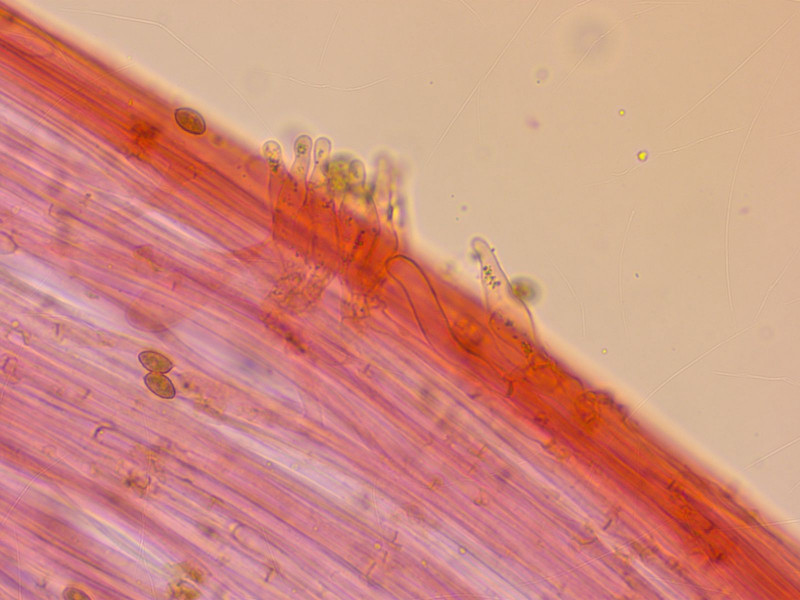
Kaulozystiden ähnlich.
7:

Ein Schüppling, scheinbar terrestrisch, vielleicht auf vergrabenem Holz: Pholiota gummosa.
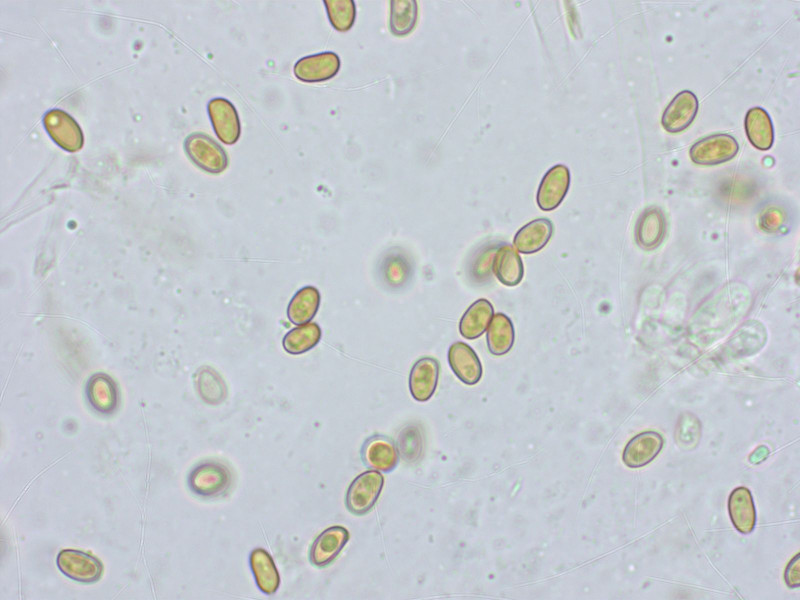
Sporen klein
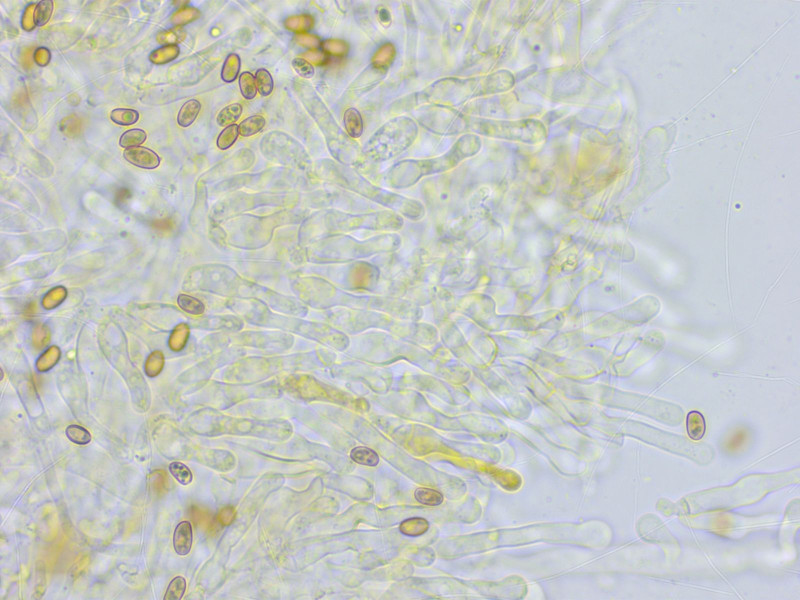
Cheilozystiden teilweise als Chrysozystiden.
8:

Porpolomopsis calyptriformis
9:

Tricholoma atrosquamosum. Später wurde die Stielbasis knallblau.
Tag 4: Ein alter Laubmischwald mit Fichten
10:

Callistosporium luteo-olivaceum
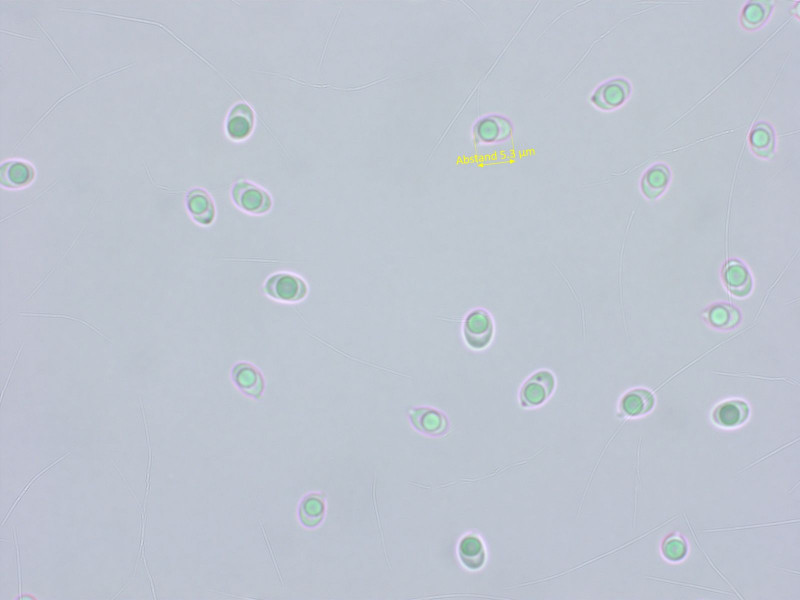
Sporen im Ammoniak mit dem typisch grünlichen Tropfen
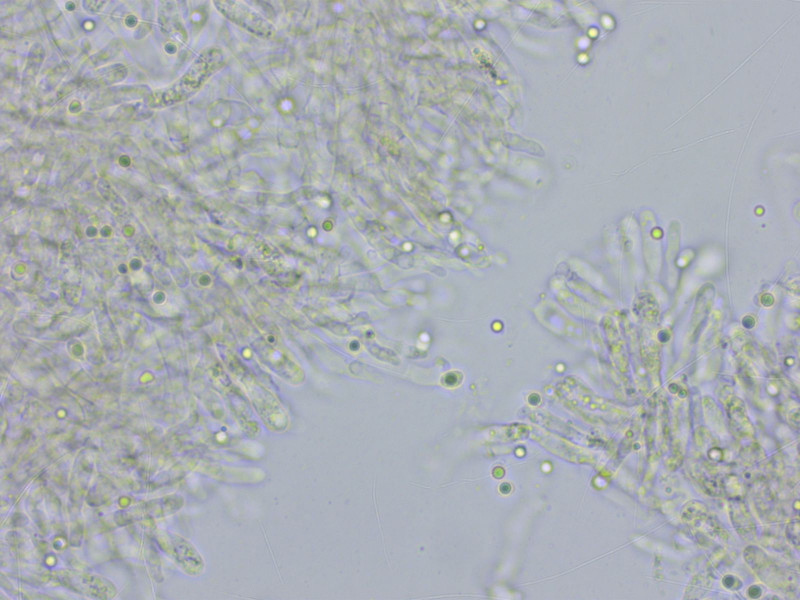
Zystidoide Elemente an der Lamellenschneide
11:

Eine Telamonia, bestimmt als Cortinarius umbrinolens.
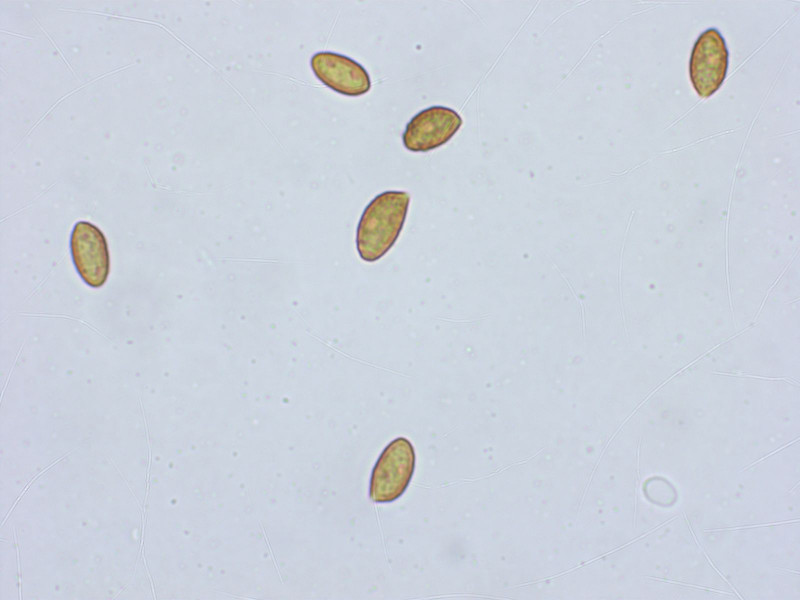
Sporen recht schlank
12:

Kleine Schirmlinge sind immer schön... das hier sollte Lepiota boudieri sein.
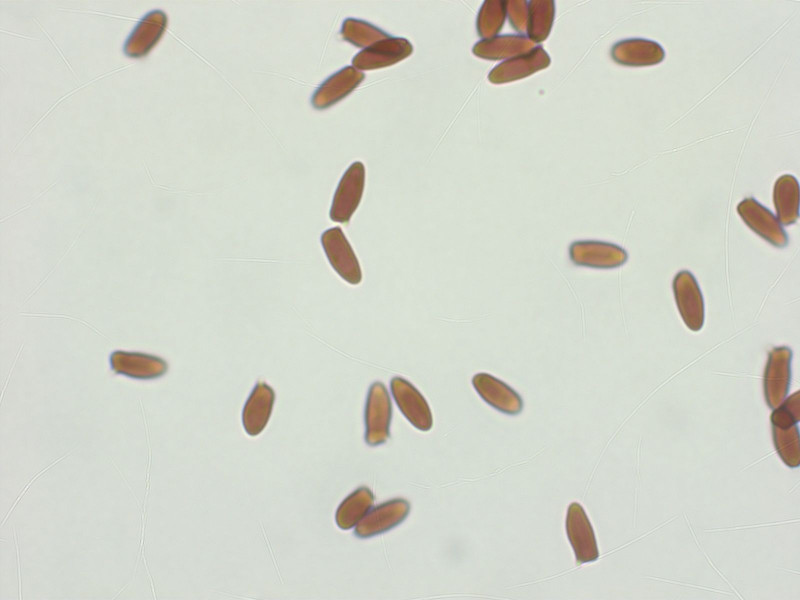
Sporen gespornt.
Tag 5: Ein Buchen-Fichtenwald
13:

Callistosporium pinicola
Schon verrückt. Die Gattung suche ich seit Jahren, und hier gab es zwei Arten in einer Woche.
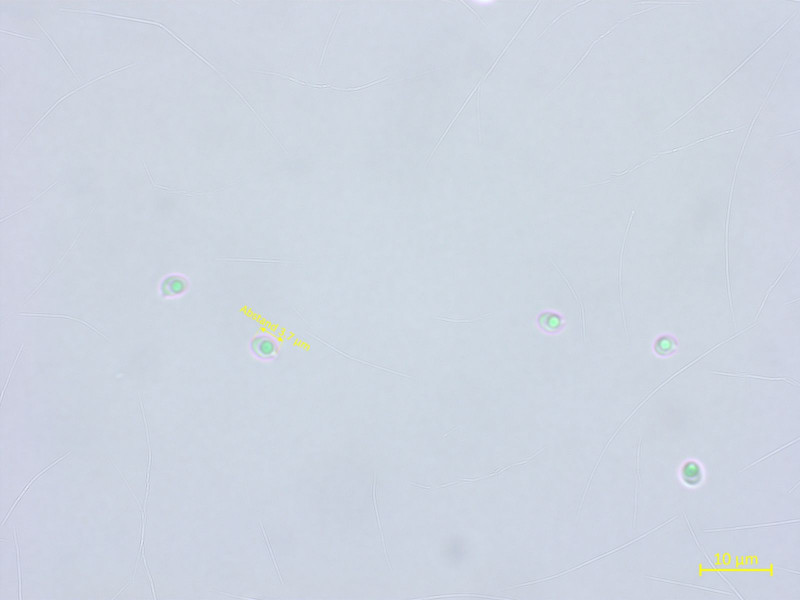
Die Sporen sind deutlich kleiner als bei C. luteo-olivaceum.
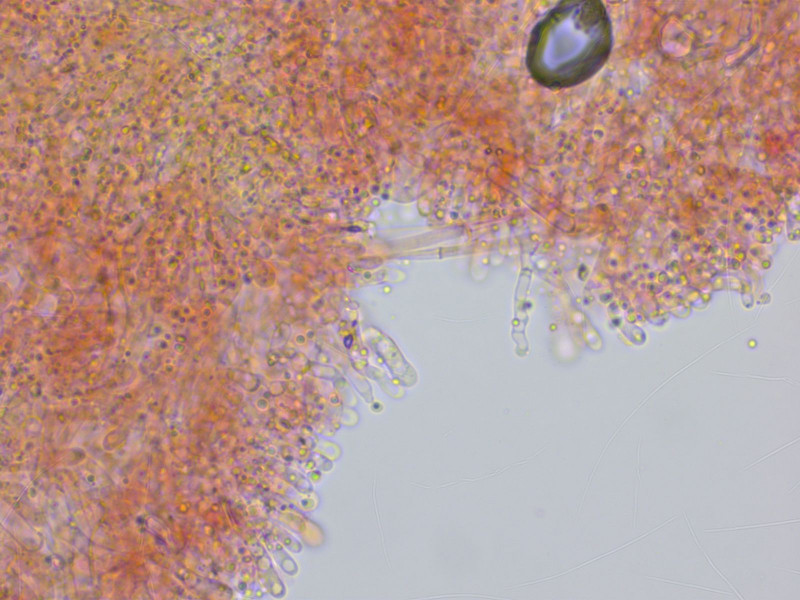
Zytidoide Elemente gab es hier auch.
14:

Cortinarius anserinus
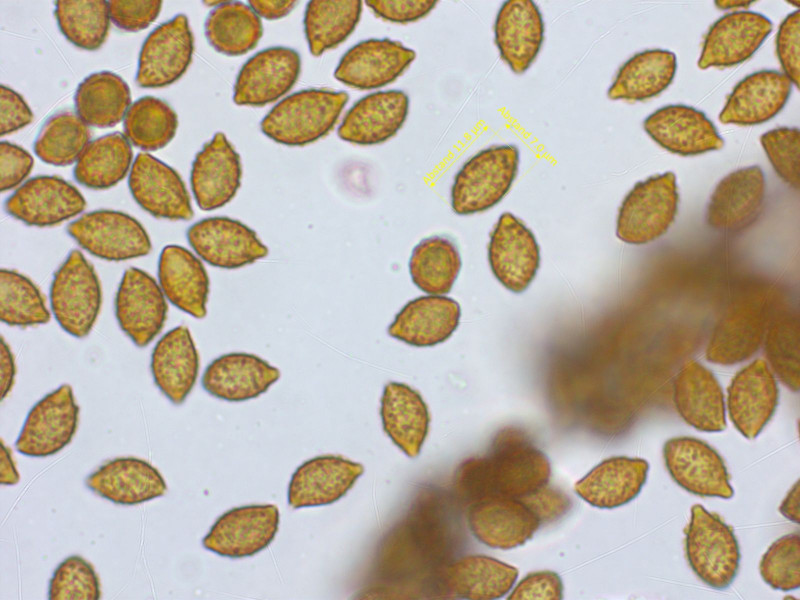
Sporen in KOH, grob wartzig
15:

Noch ein dunkelstieliger Häubling auf Holz, aber das ist ein anderer: Galerina camerina
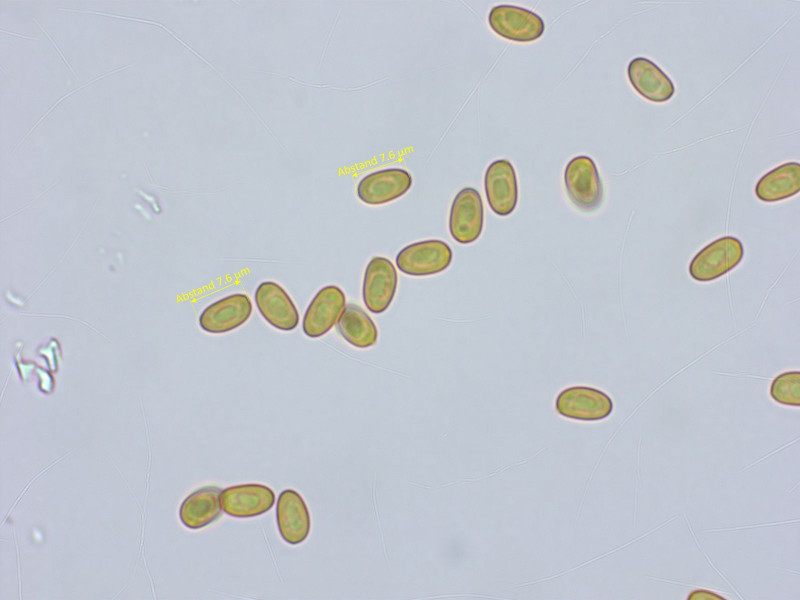
Sporen glatt, zumindest im Lichtmikroskop.
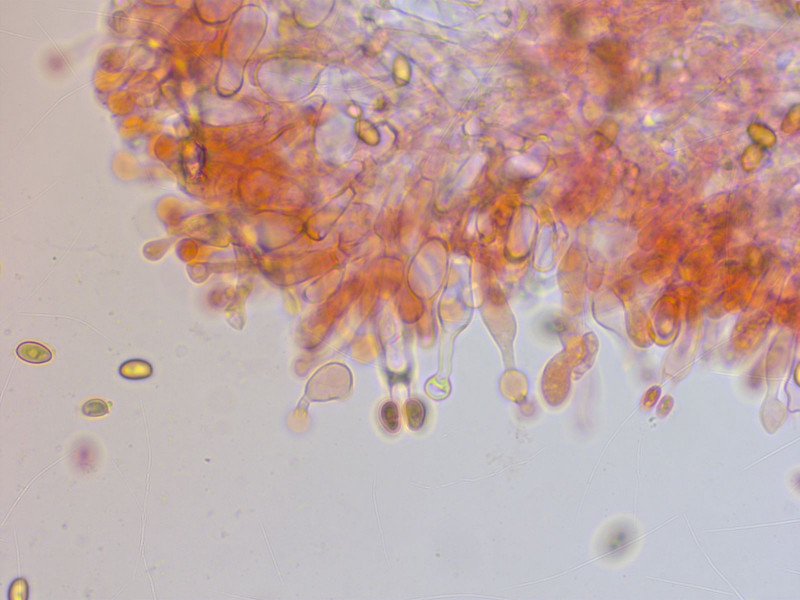
Cheilozystiden kopfig.
16:

Gymnopilus bellulus, immer wieder schön. Es gibt jetzt auch einen Gymnopilus subbellulus, der ist es aber nicht.
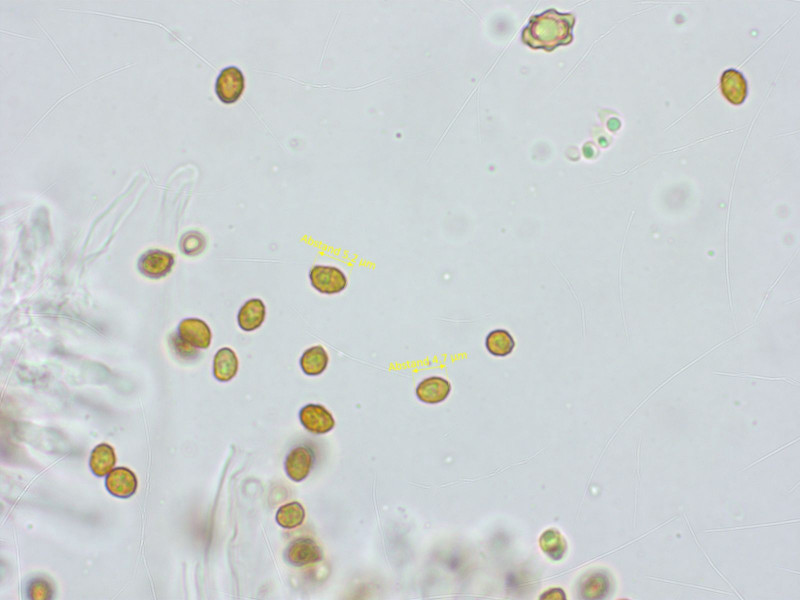
Sporen winzig
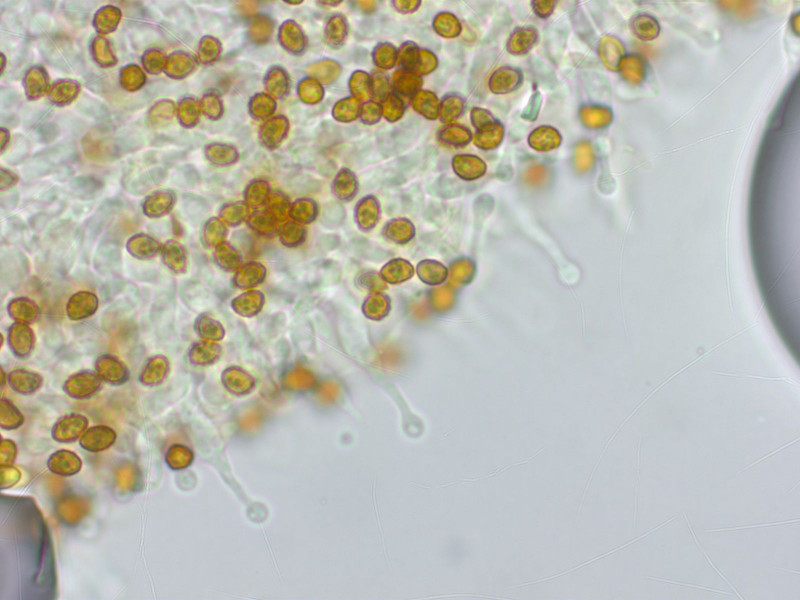
Zystiden kopfig.
17:

Ein kleiner Risspilz, der auch makroskopisch ansprechbar ist: Inocybe petiginosa.
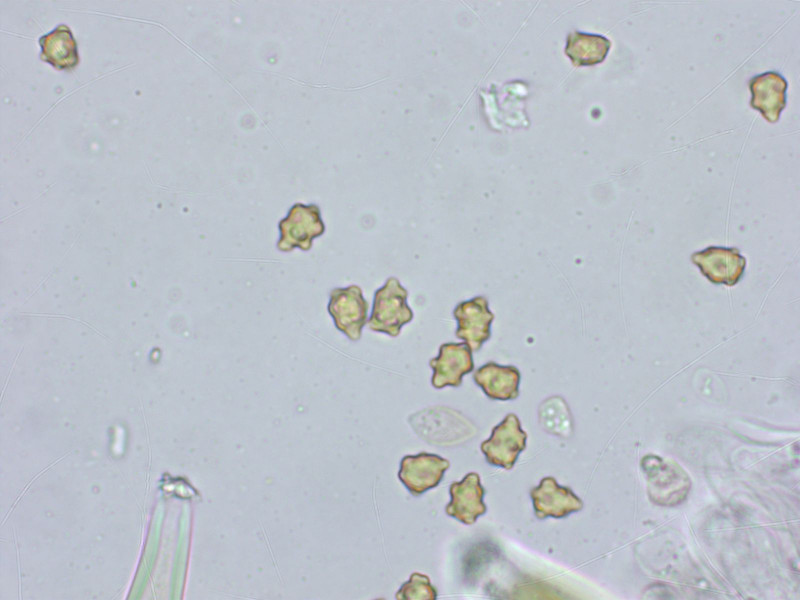
Sporen höckerig und klein.
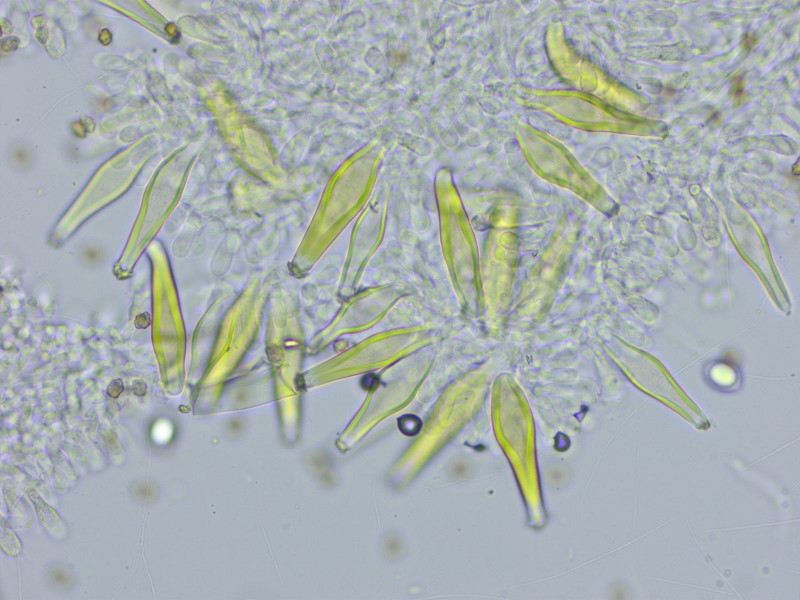
Die Zystiden sind in KOH wunderschön gelb.
18:

Tricholomopsis decora, schön im Vergleich zu Tr. sulfureoides oben.
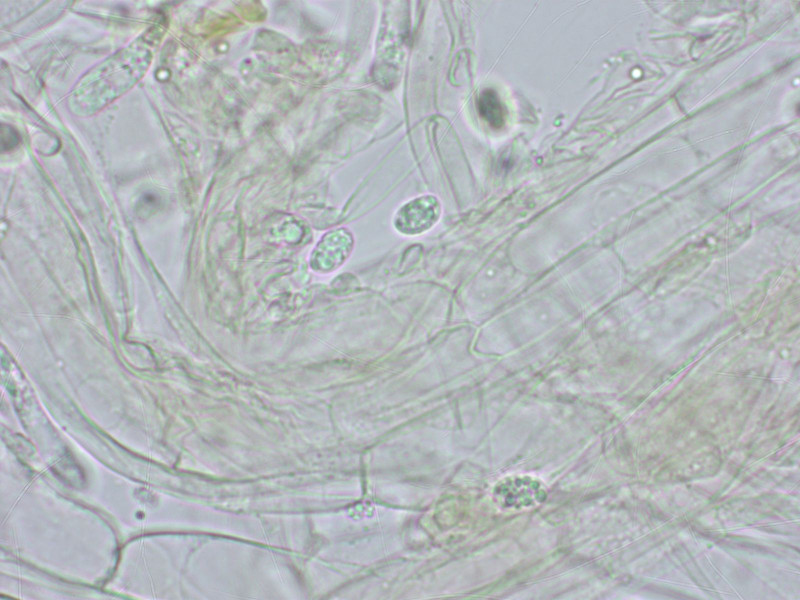
Den Sporenabwurf haben sie verweigert.
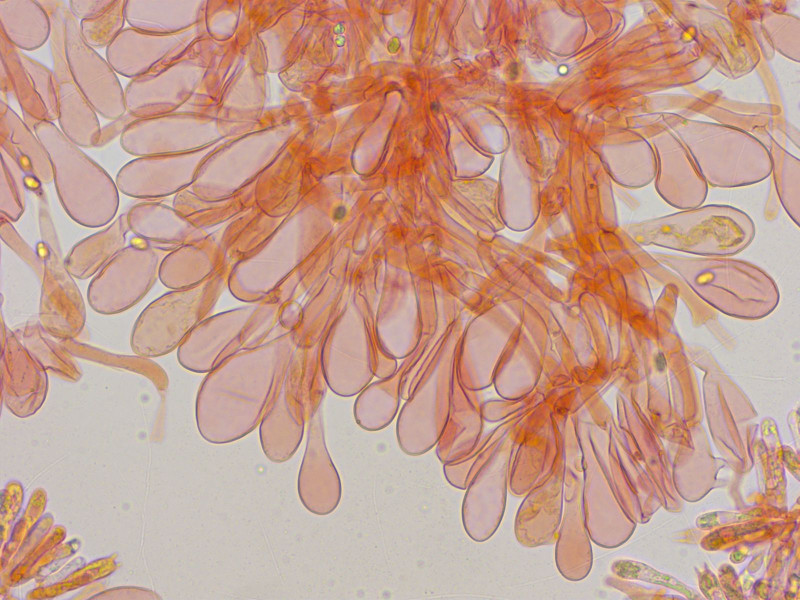
Zystiden breit keulig.
Tag 6: Trockenrasen mit Pinus sylvestris auf dem Heimweg
19:

EIn kleiner Nabelrötling, dazu sollte in Kürze ein neues Paper herauskommen.
Im Moment nenne ich es mal Entoloma flocculosum.
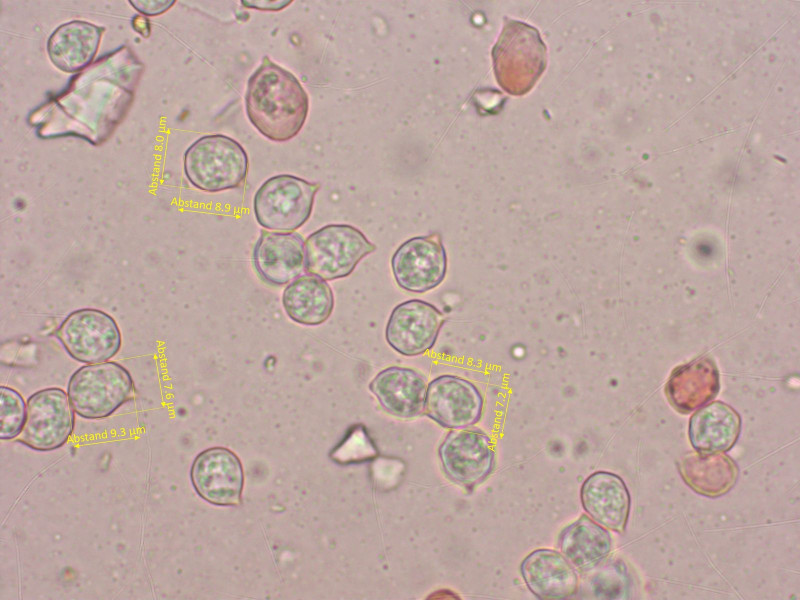
Sporen mehr oder weniger isodiametrisch.
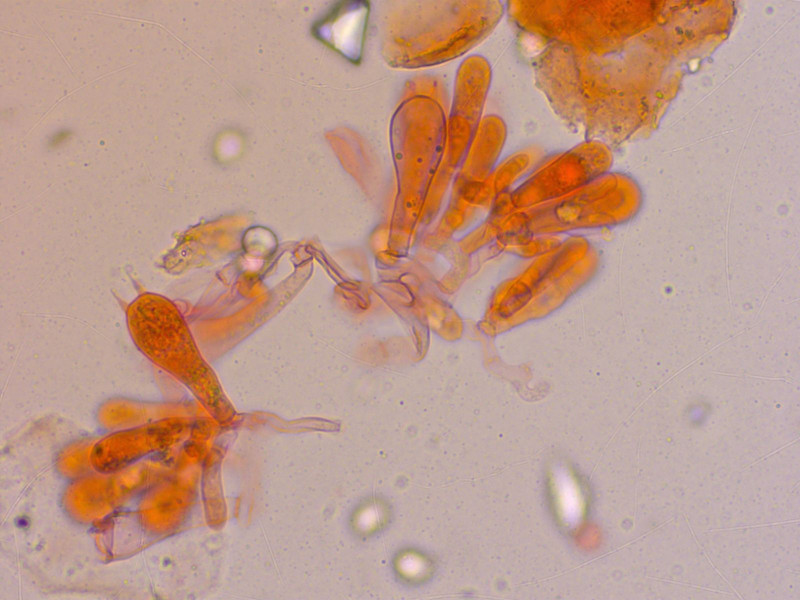
Basidien 4sporig, ohne Schnallen, keine Zystiden.
20:

Noch so ein Rötling, man könnte meinen es ist der gleiche, aber nein: Entoloma cf. phaeocyathus.
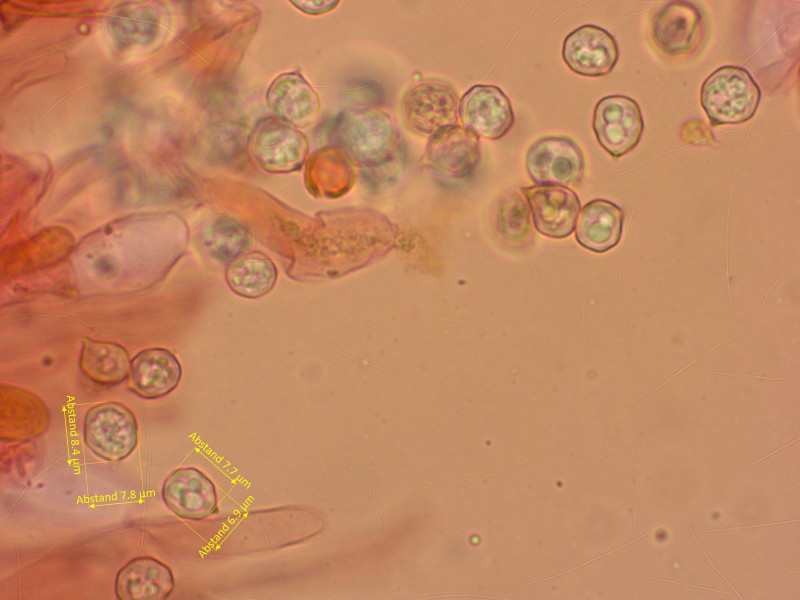
Sporen wieder fast isodiametrisch.
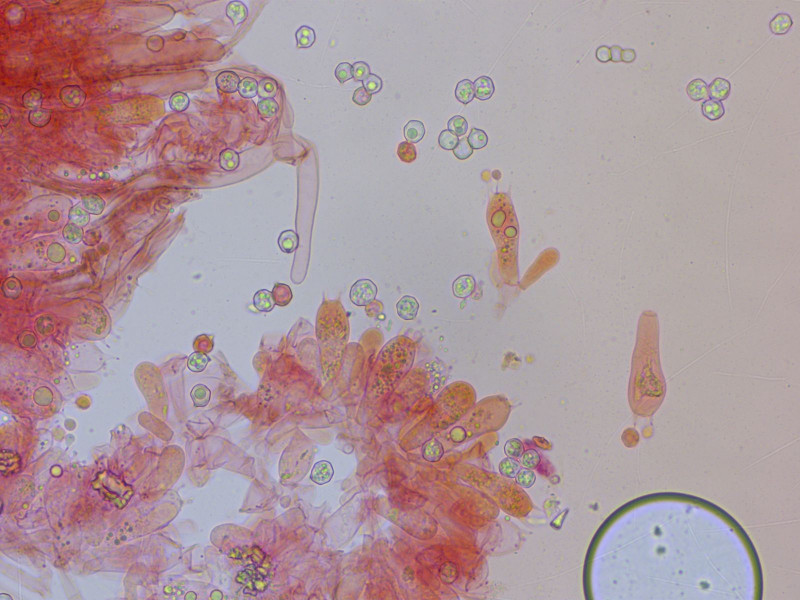
Basidien 4sporig, ohne Schnallen.
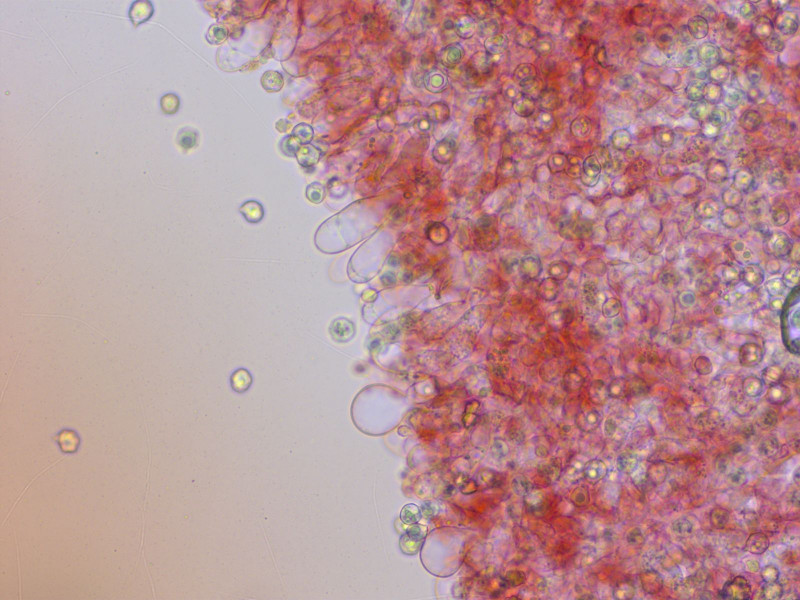
An der Schneide gibt es zahlreiche zylindrische oder blasige Zystiden.
21:

Rhodocybe caelata mit dem typisch radial-rissigen Hut.
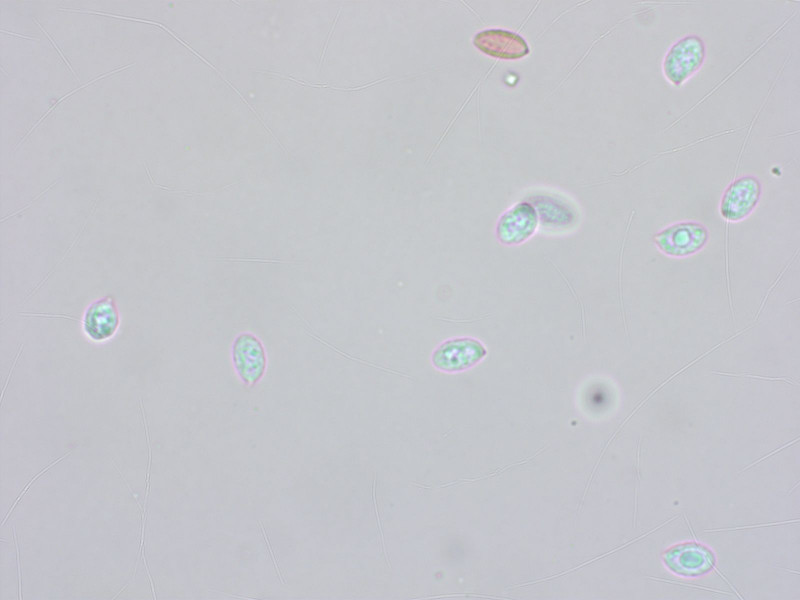
Sporen höckerig, wie es sich gehört.
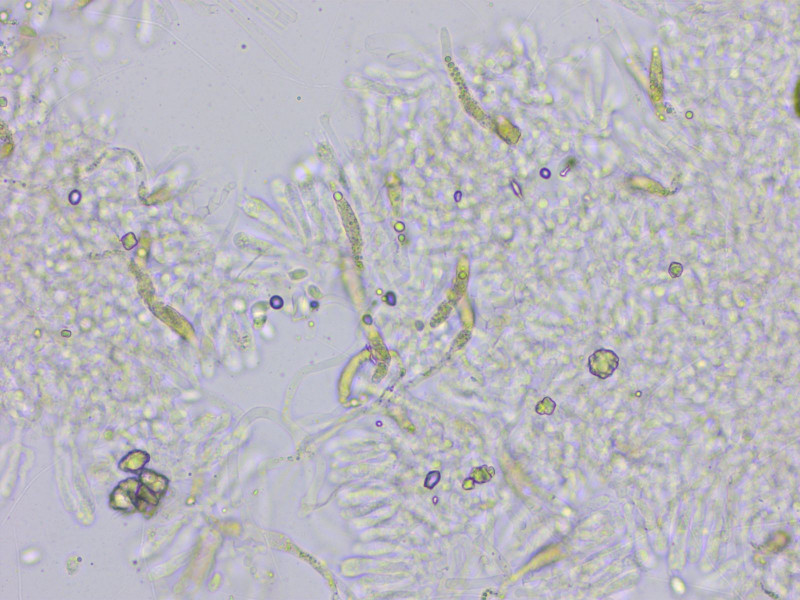
Pseudozystiden in KOH
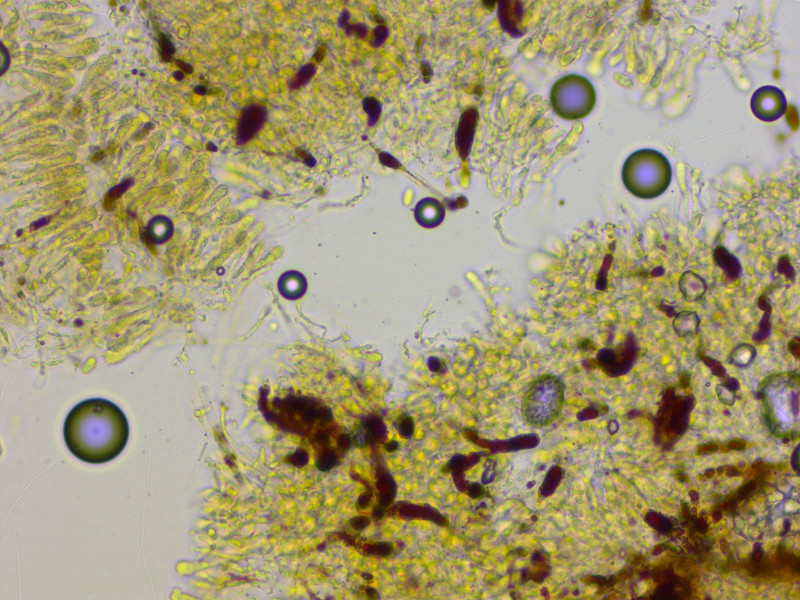
Die Pseudozystiden sind stark dextrinoid, schwarzbraun in Melzer.
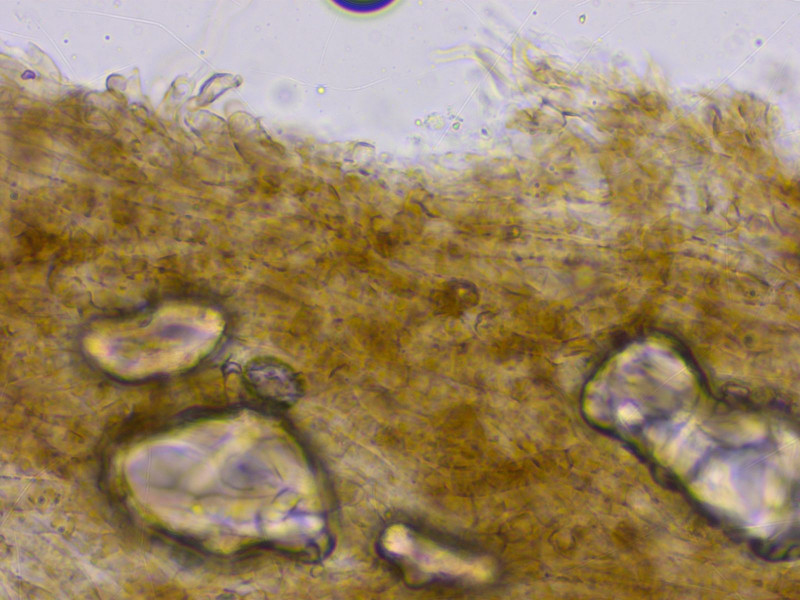
HDS deutlich inkrustiert.
22:

Eine unbestimmbare Rhodocybe aus dem caelata-Aggregat.
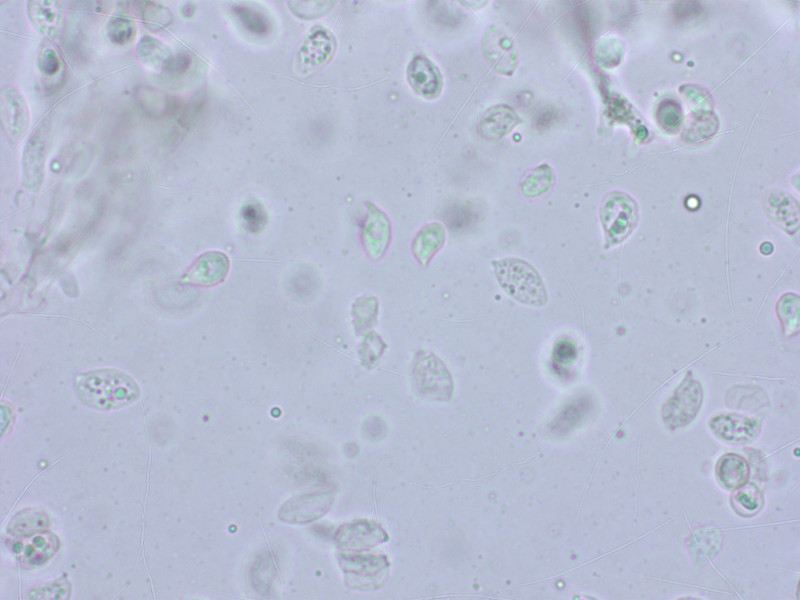
Sporen wie oben.
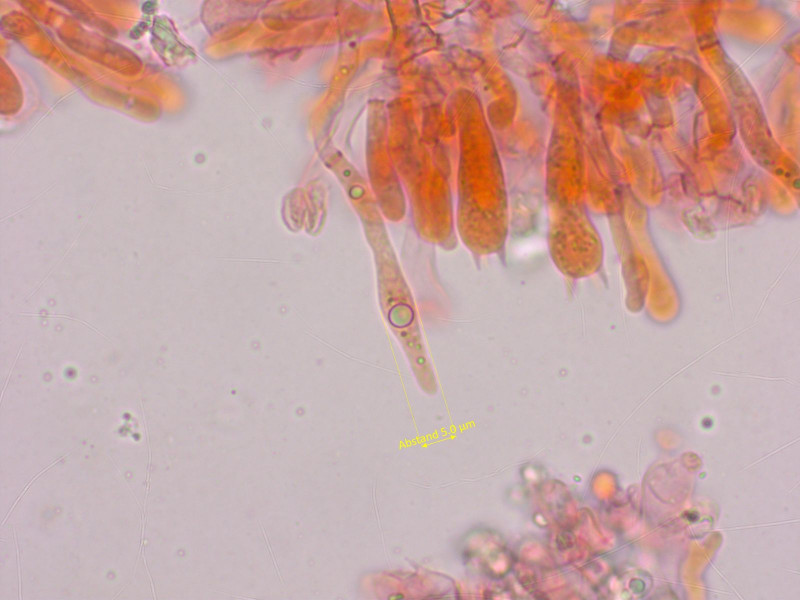
Wieder mit schlank fusiformen Pseudozystiden.

Die sind auch wieder stark dextrinoid.
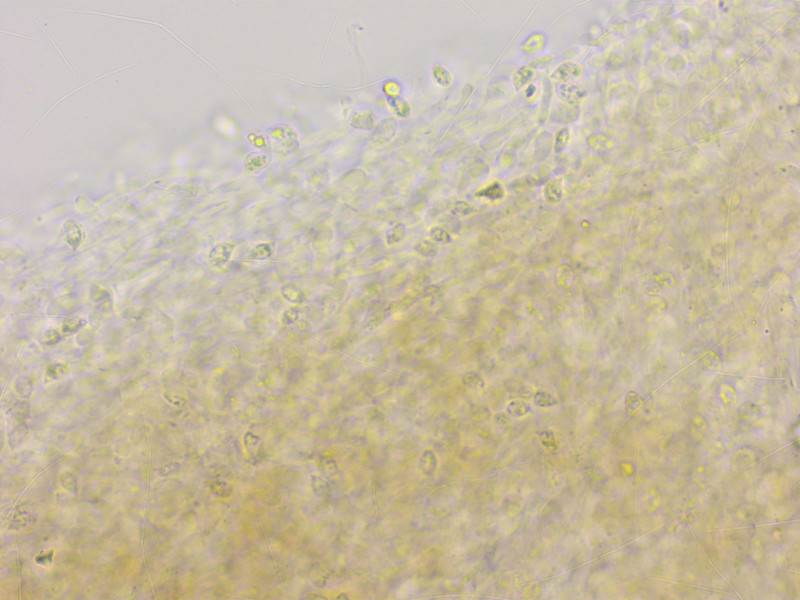
HDS kaum inkrustiert, dafür aber gelatinisiert.
23:

Rhodocybe zum Dritten, dieses Mal wieder bestimmbar: Rhodocybe brunnea.
Die Art wurde aus Sardinien beschrieben, kommt aber hier auch vor.
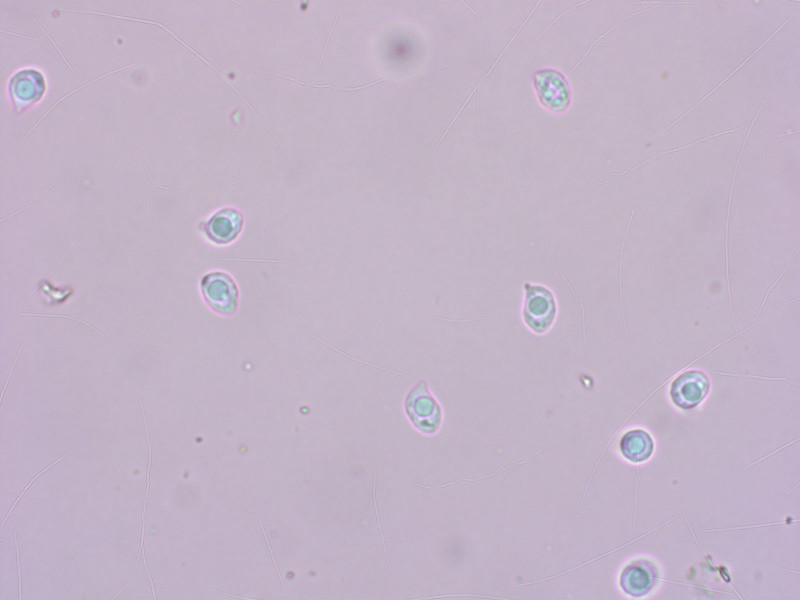
Die Sporen helfen nicht weiter.
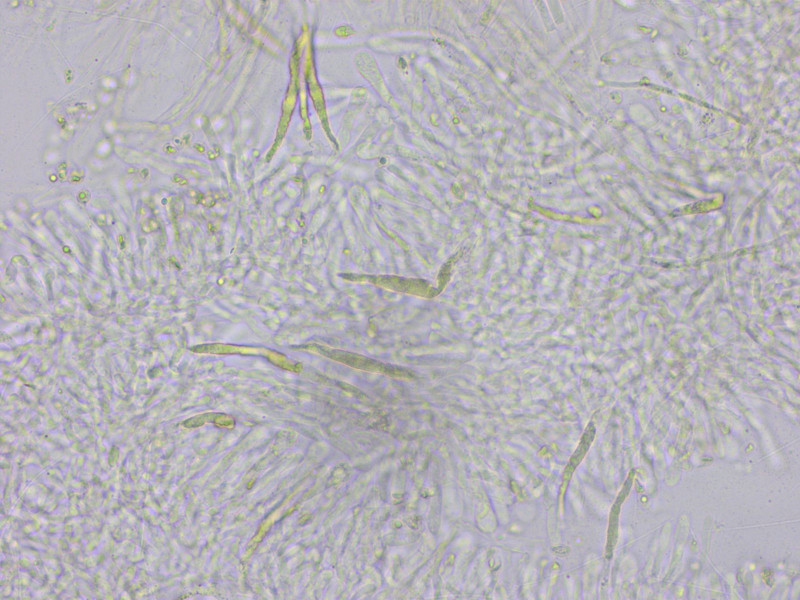
Pseudozystiden hat er auch.
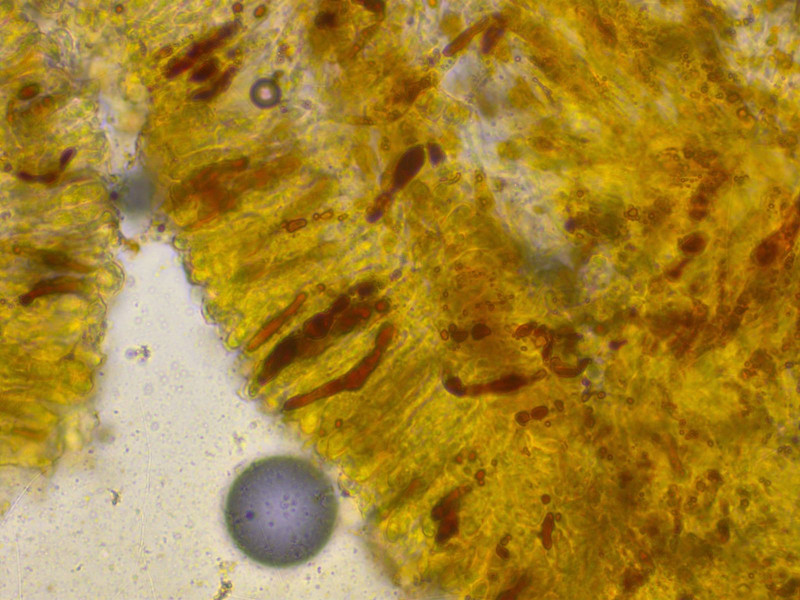
Aber dieses Mal sind sie viel schwächer dextrinoid.
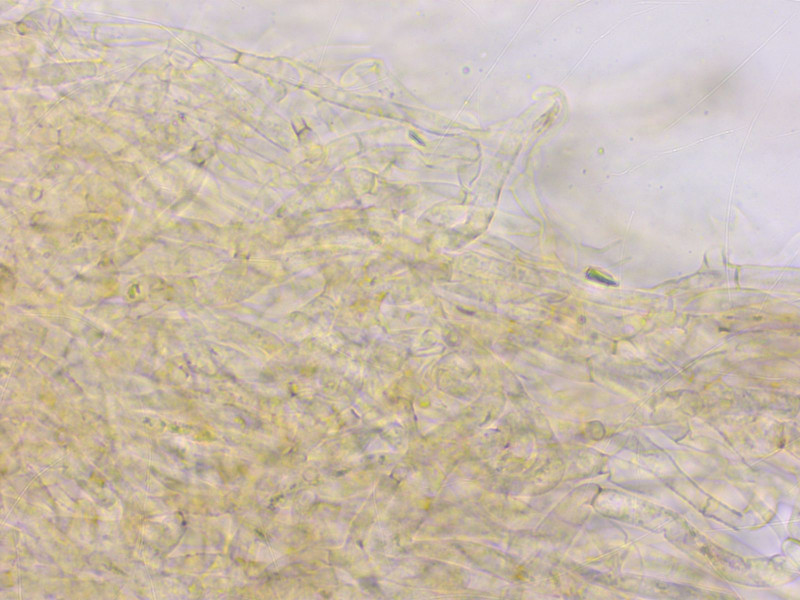
Die HDS ist leicht inkrustiert.
Korrekturen/Fragen immer willkommen.
LG Raphael


