Hallo zusammen,
nachdem ich vor einer Woche schon eine Vorexkursion in Ennepetal durchgeführt hatte, ging es gestern mit der gesamten Kompetenz des Mykologischen Arbeitskreises Bergisches Land noch einmal dorthin und zwar ins NSG Kluterthöhle. Dabei fanden sich einige der Arten der Vorwoche wieder, daneben aber auch viele neue Arten, die ich bei meinem Schnelldurchlauf in der Vorwoche übersehen hatte. Und kurz vor Ende der Exkursion gab es dann noch ein lilanes Highlight:
1. Ramaria stricta



2. Artomyces pyxidatus


3. Haareis in rauen Mengen






4. Mycena capillaris

5. Clavulina cinerea

6. Hygrophorus eburneum


7. Macrotyphula fistulosa

8. Kann ich den Fund also Mycoacia/Phlebia uda ablegen? Mit 3% KOH verfärbte der Fruchtkörper rötlich
Kluterthöhle-0024.jpg




9. Polyporus varius mit Schleimpilz

10. Ein Highlight des Tages: Tricholoma portensum


11. Bisporella citrina




12. Pseudoclitocybe cyathiformis

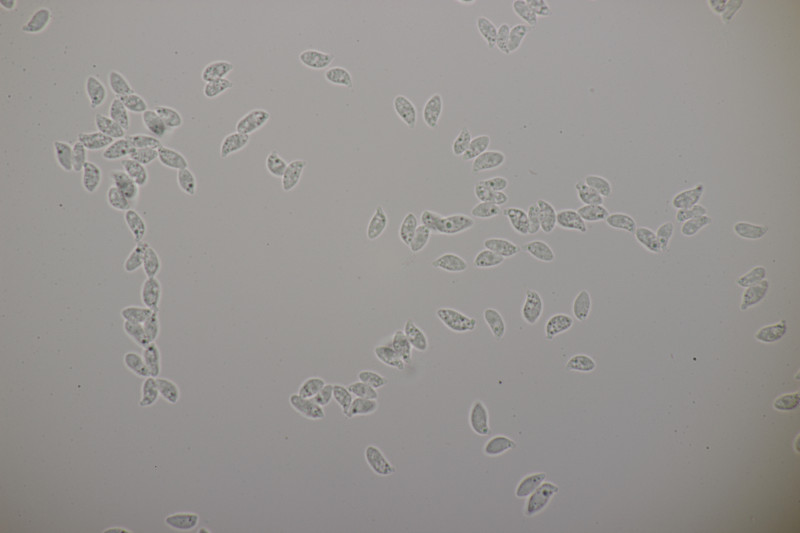
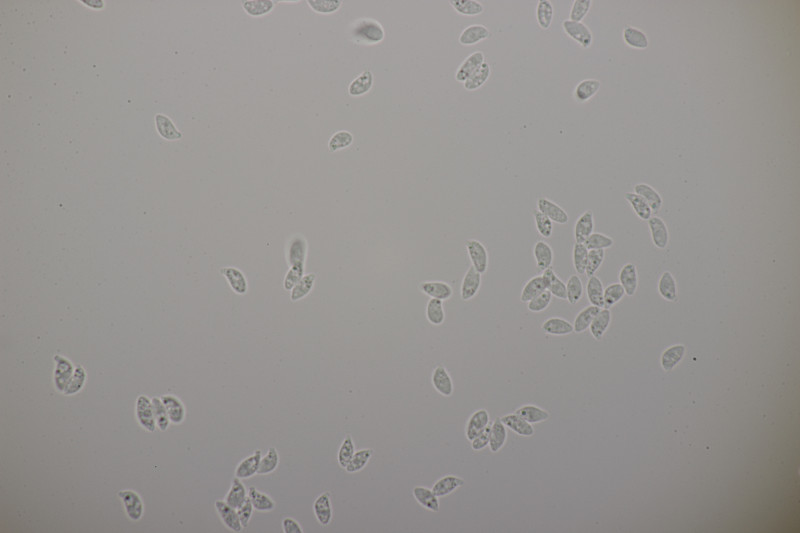
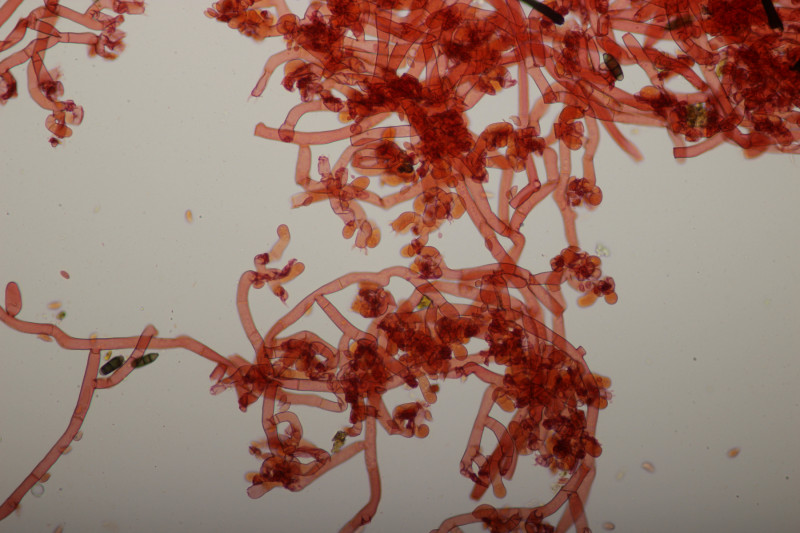
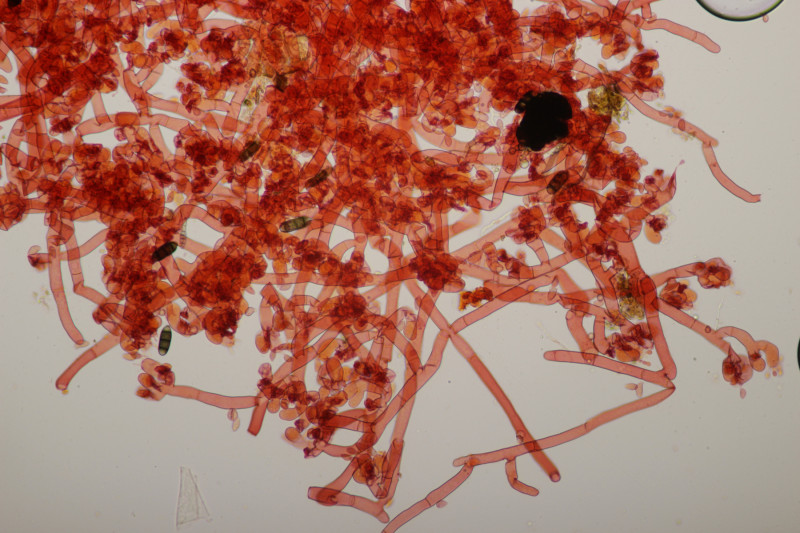
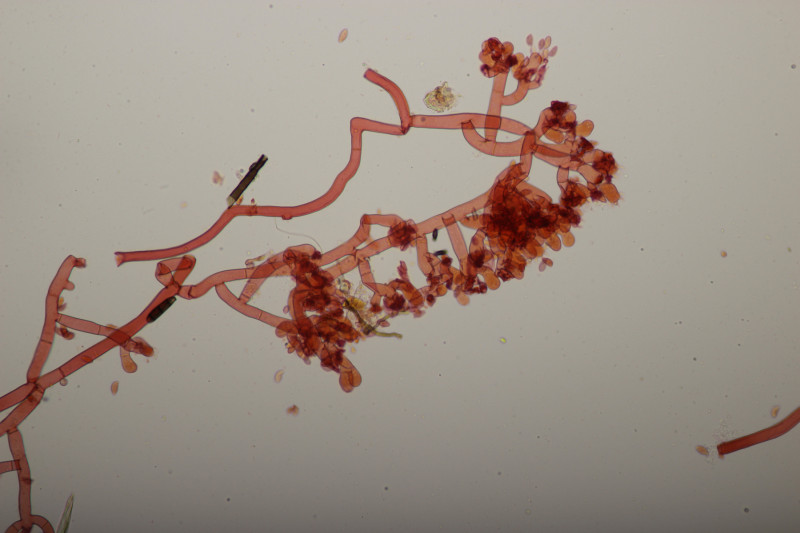
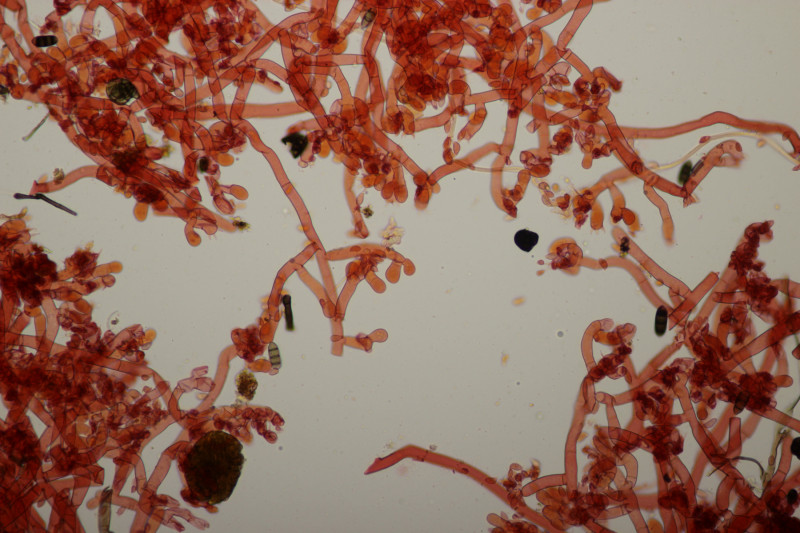
13. Botryobasidium vagum, Sporengröße (8.6+-0.7) µm x (3.9+-0.2) µm, Q=2.2+-0.2




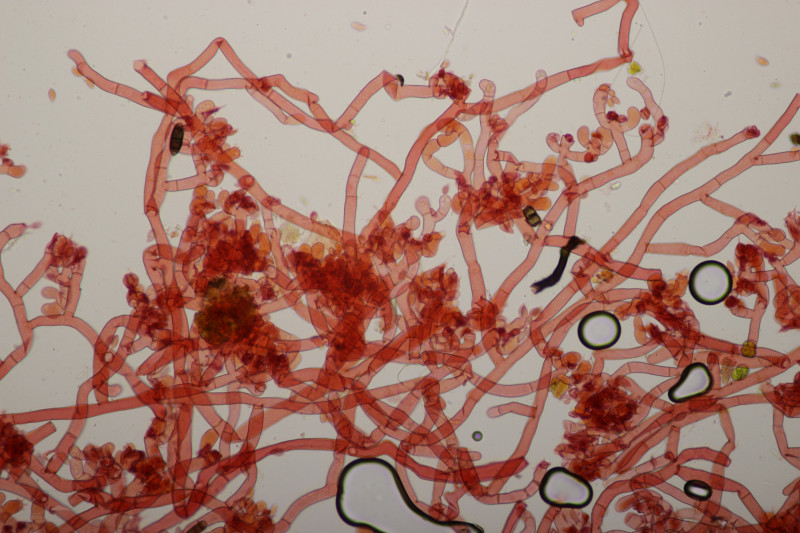
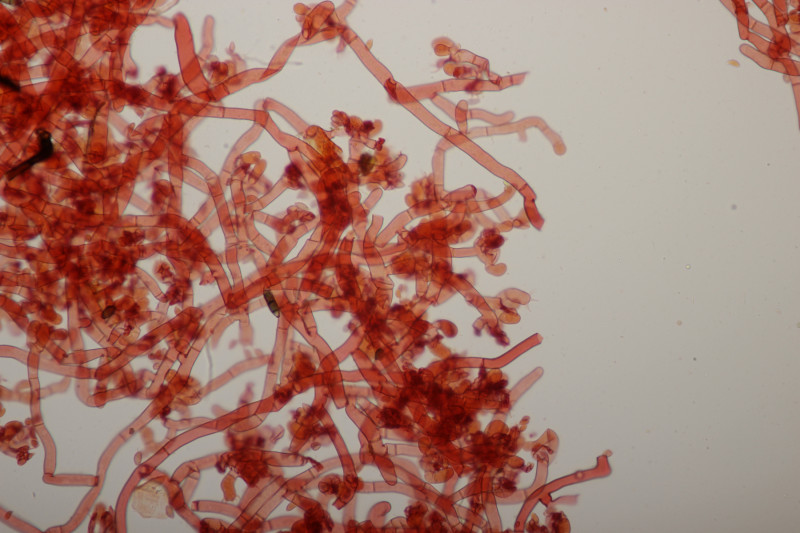
14. Lycoperdon echinatum

15. Trichia decipiens

16. Und wenn es Schleimpilze gibt, ruft man natürlich mal Jan-Arne. Der war einen Blick auf den Stamm und war vor Freude fast nicht mehr einzufangen: Enerthenema papillatum. Wohl kein besonders seltener Fund, aber einer, dem er schon seit Jahren hinterherrennt.


17. Phlebia radiata

18. Tricholoma lascivum

19. Chromocyphella muscicola

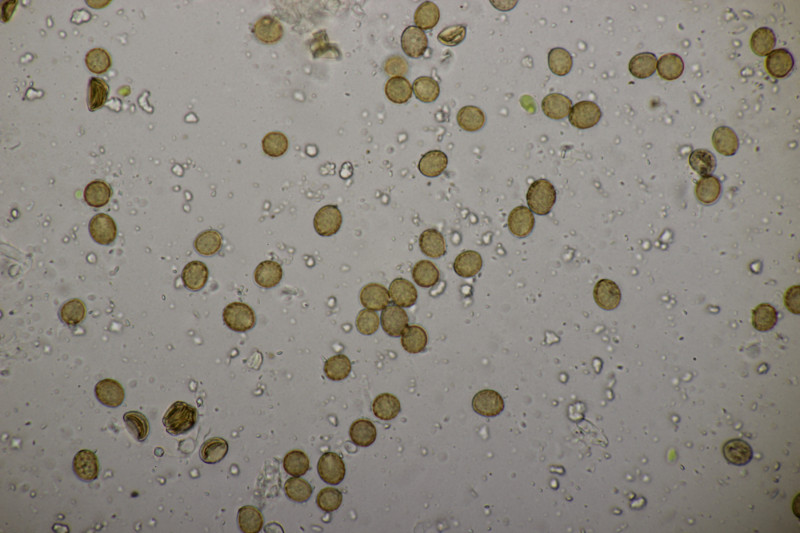
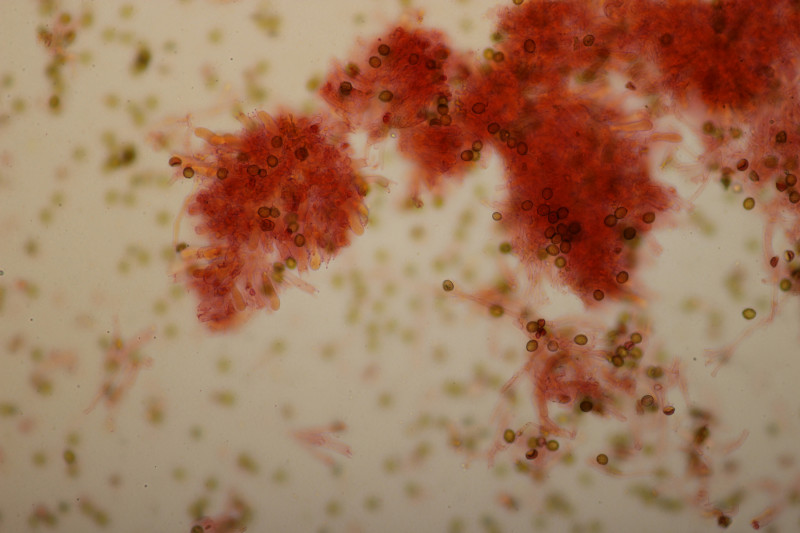

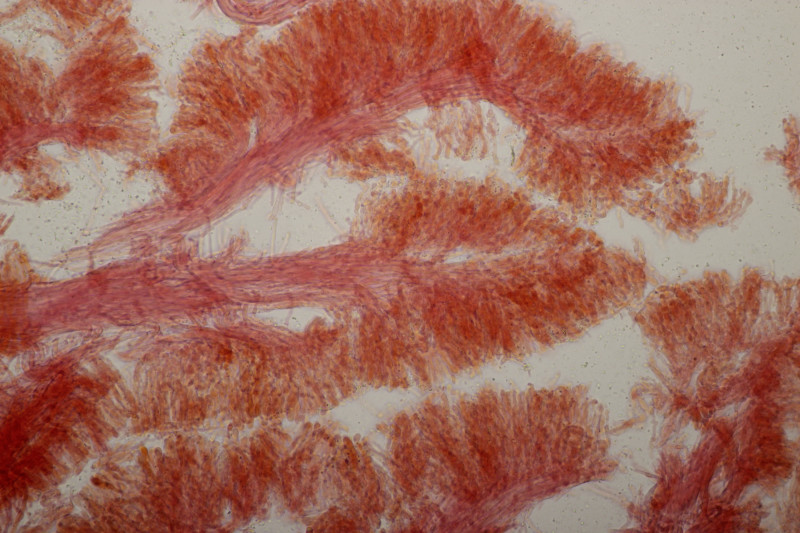
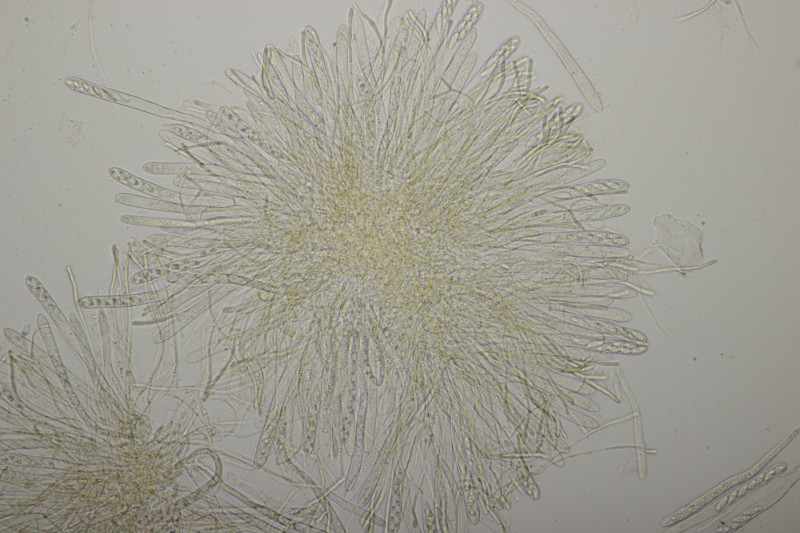
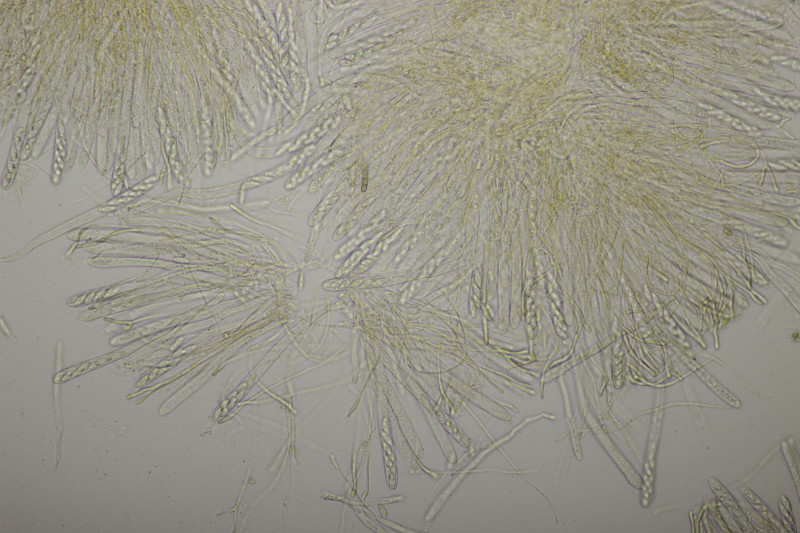
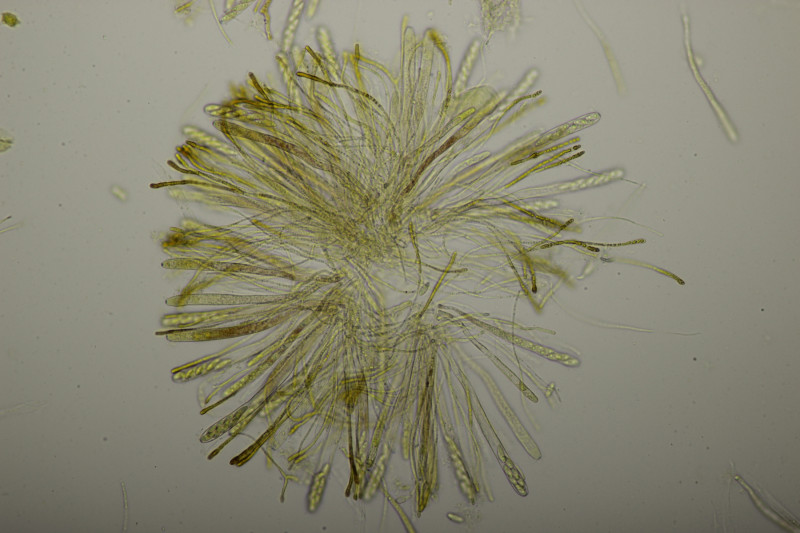
20. Arachnopeziza aurata an gleicher Stelle wie letzte Woche



21. Auch ein Wiederfund: Tomentella neobourdotii


22. Cortinarius sp. bei Buche und Eiche

23. Marasmius wynneae


24. Es wird cyphelloid!


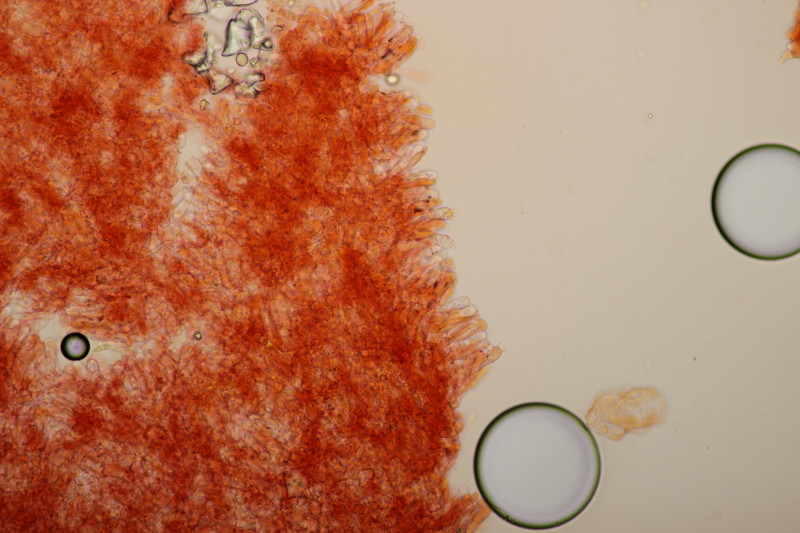

25. Clavulina rugosa

26. Hygrocybe cantharellus

27. Chromosera viola, ein extrem seltener Saftling mit gerade mal 7 Fundstellen in Deutschland - davon 6 in NRW.


28. Hygrocybe glutinipes

29. Ein Rißpilz, den sogar ich bestimmen kann: Inocybe lilacina

30. Hypomyces microspermus mit Sporen von 9.0 bis 12.8 µm


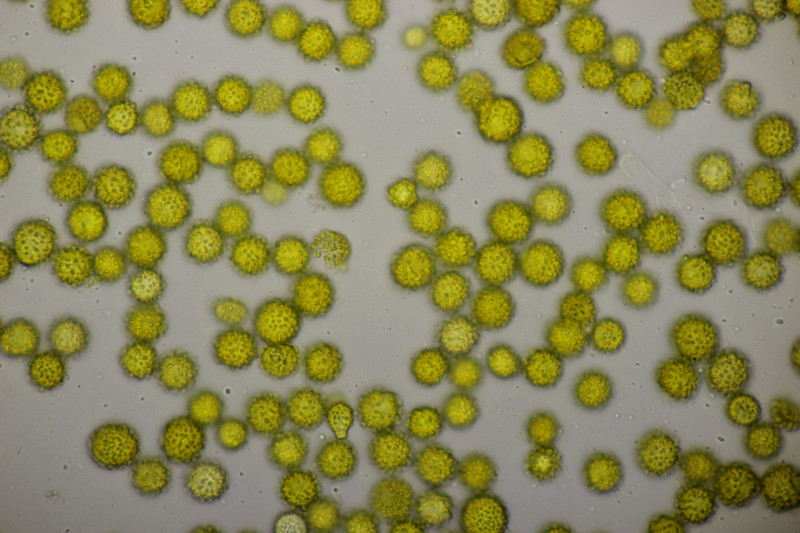
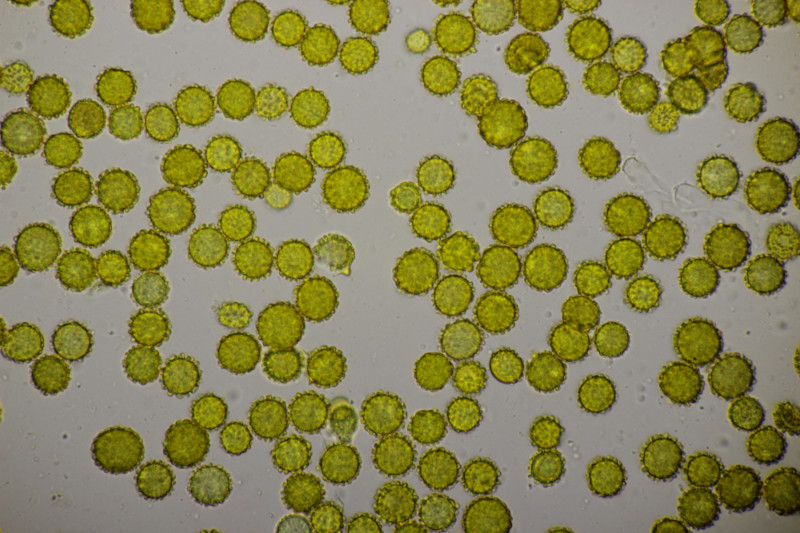
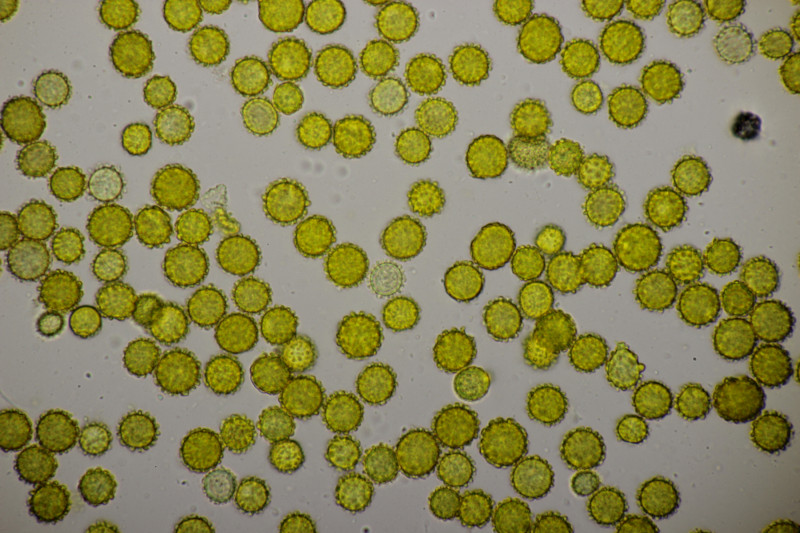
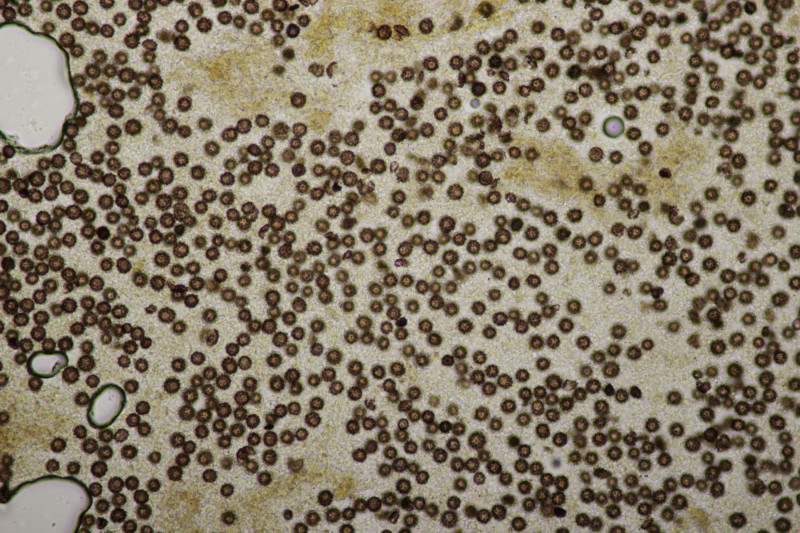
31. Stachelige Sporen mit Sporengrößen von 7.7-10.5 µm, damit lande ich bei Scleroderma verrucosum
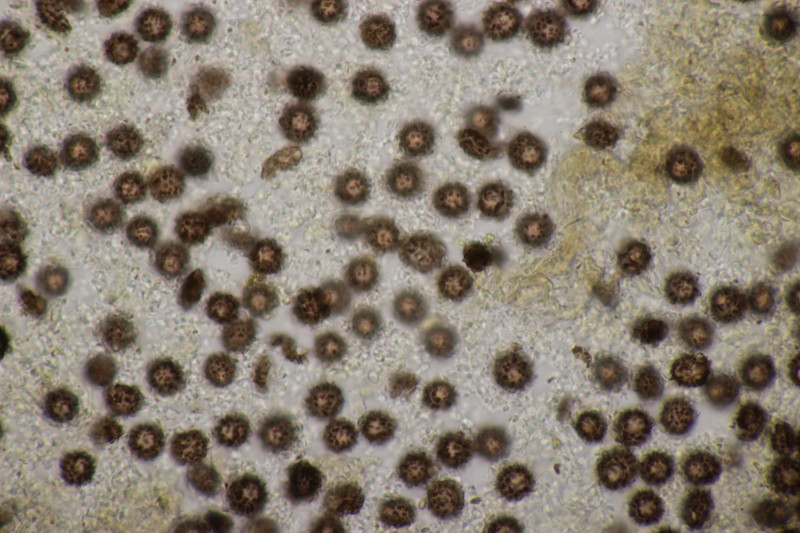
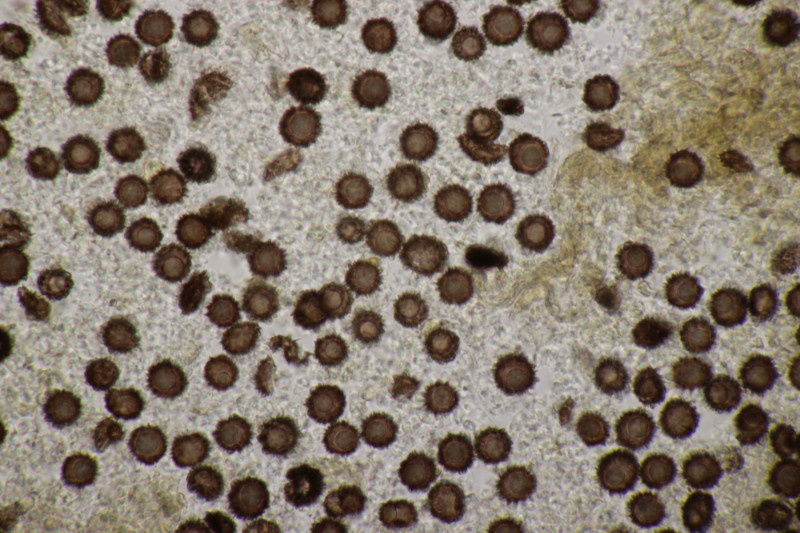
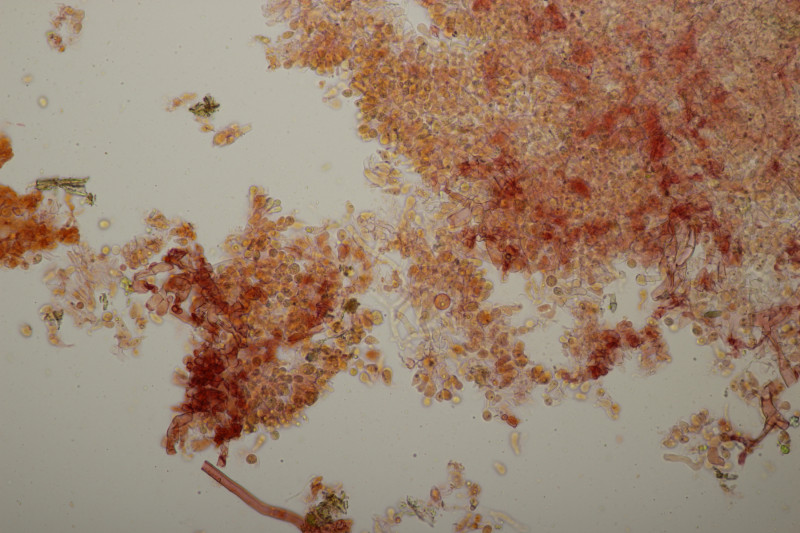
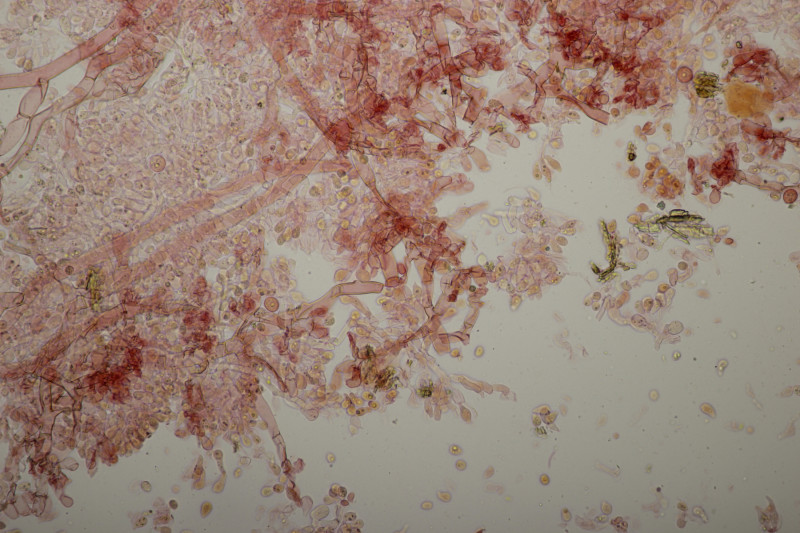
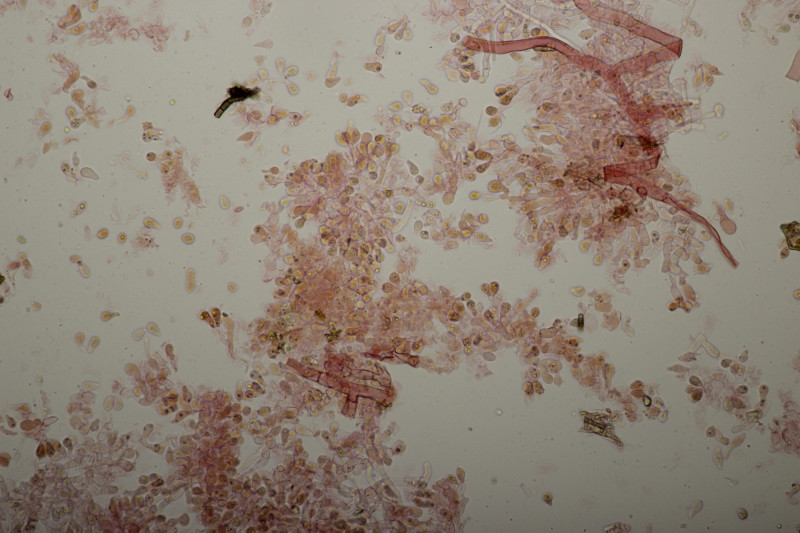
32. Tulasnella violea

Björn
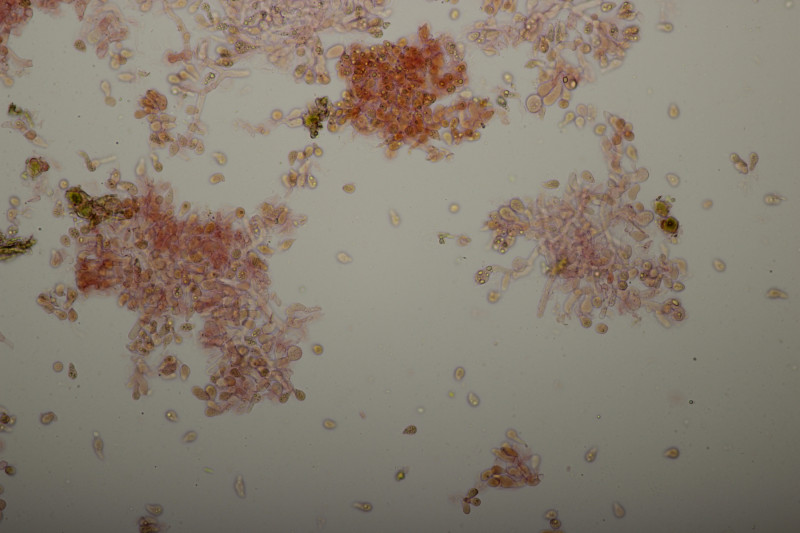
![]() Auf meinen Fotos ist dann halt das übliche Problem mit der Schärfentiefe. Man kann das mit den 8 Sterigmen aber erahnen. Auf dem letzten Bild sieht man ja Basidien, bei denen man 4 Sterigmen erkennt, das ist dann quasi nur die vordere Hälfte und dahinter geht es noch mal genau so weiter.
Auf meinen Fotos ist dann halt das übliche Problem mit der Schärfentiefe. Man kann das mit den 8 Sterigmen aber erahnen. Auf dem letzten Bild sieht man ja Basidien, bei denen man 4 Sterigmen erkennt, das ist dann quasi nur die vordere Hälfte und dahinter geht es noch mal genau so weiter.

