Hallo zusammen,
am Samstag habe ich auf dem Weg zu meinen Eltern einen kleinen Zwischenstop im Gleispark Frintrop in Essen eingelegt. Früher war das mal ein riesiger Rangierbahnhof, mittlerweile sind die Gleise alle weg und das ganze wurde parkartig ausgestaltet, hat aber immer noch den Charakter einer Industriebrache. Als ich dort unterwegs war, traf ich einen älteren Herren, der mich fragte, ob ich dort etwas Seltenes finden würde. Ich hab ihm gesagt, daß ich nach Pilzen suche. "Pilze gibt's hier nicht. Hier ist nur Dreck im Boden." Dann hab ich ihm ein paar kleine, vertrocknete Anistrichterlinge gezeigt. "Hmm, ja gut. Aber hier wächst nichts, alles nur voller Dreck unten drunter". Jetzt also eine Auswahl, der Dreckspilze, die es da gar nicht gibt 
1. Paxillus sp. unter Birke. Ich hab bei meinen Eltern einen Sporenabwurf gemacht (leider kein Foto davon). Das war dann ein typisches Rostpilz-Uredien-braun. Aber ob das jetzt rot genug war für P. cuprinus? Der Abdruckk blieb bei meinen Eltern und ich hab dann zu Hause versucht, noch mal mehr Sporen zu bekommen um auch mikroskopisch reinzuschauen. Das sah heute morgen noch nicht wirklich vielversprechend aus, aber mal schauen, ob sich im Mikro dann doch noch Sporen finden.

2. Pucciniastrum epilobii ex Epilobium angustifolium


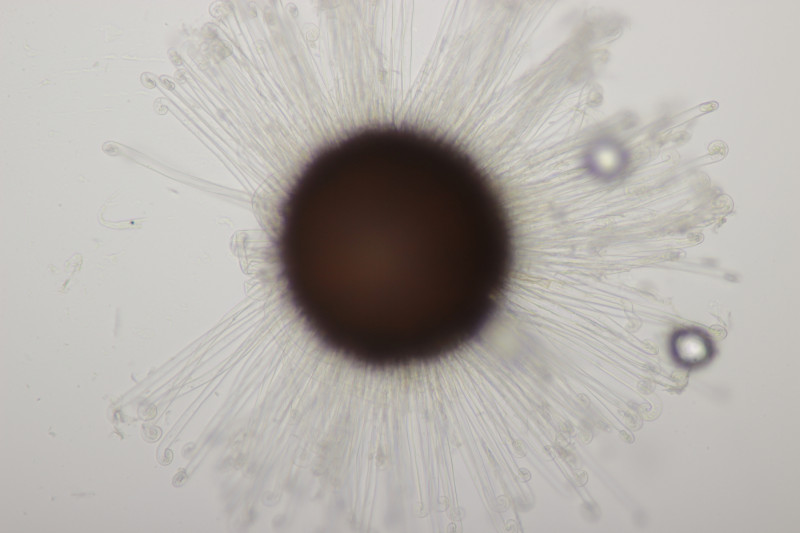
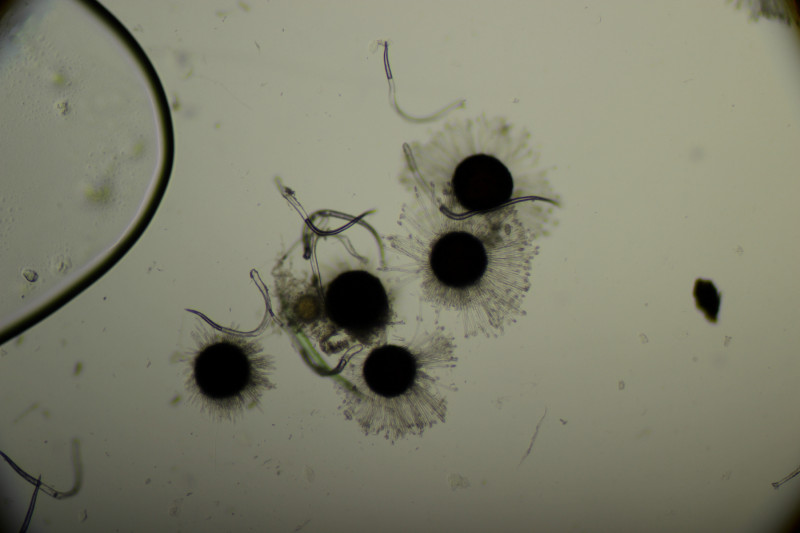
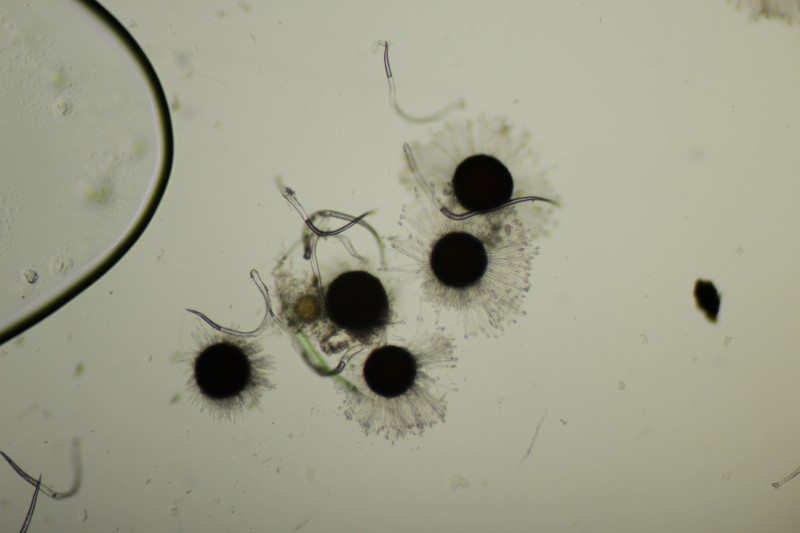
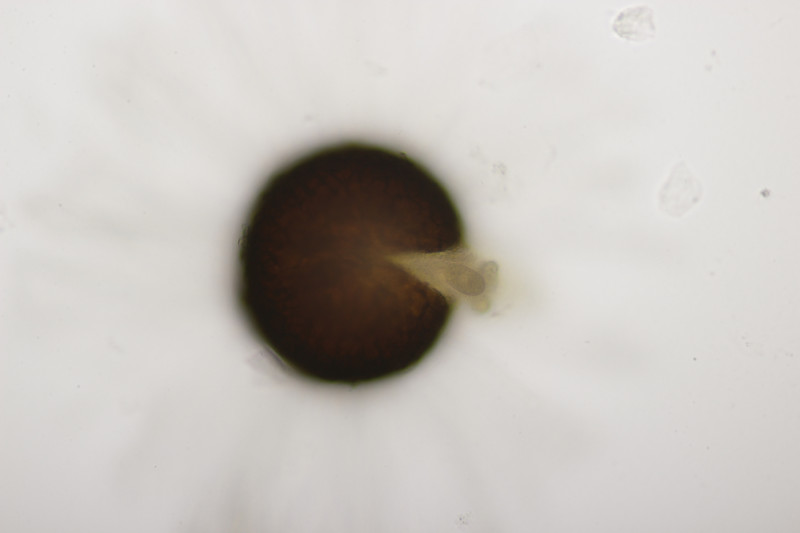
3. Weide meide gilt ja eigentlich in jeglicher Hinsicht, aber ich habe trotzdem einen Versuch gewagt. Die Fruchtkörper sind um die 170 µm groß, also genau im Überlappungsbereich von Erysiphe pseudoregularis und Erysiphe capreae. Erysiphe adunca würde ich wegen der Anhängsellänge ausschließen. Die Asci hatten dann durchgehend 5-6 Sporen, was für E. capreae sprechen würde.





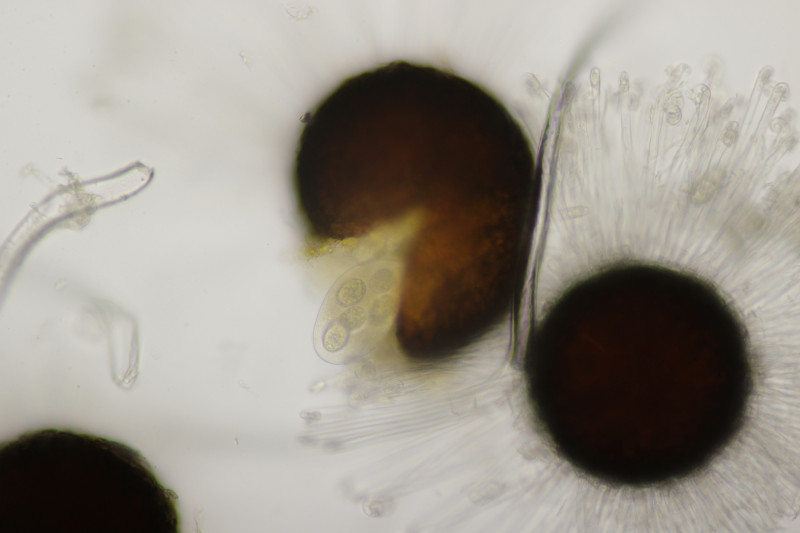
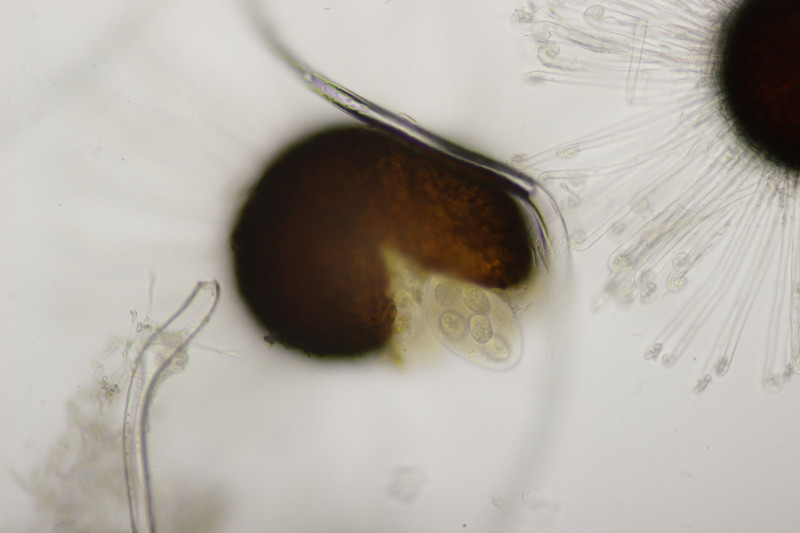

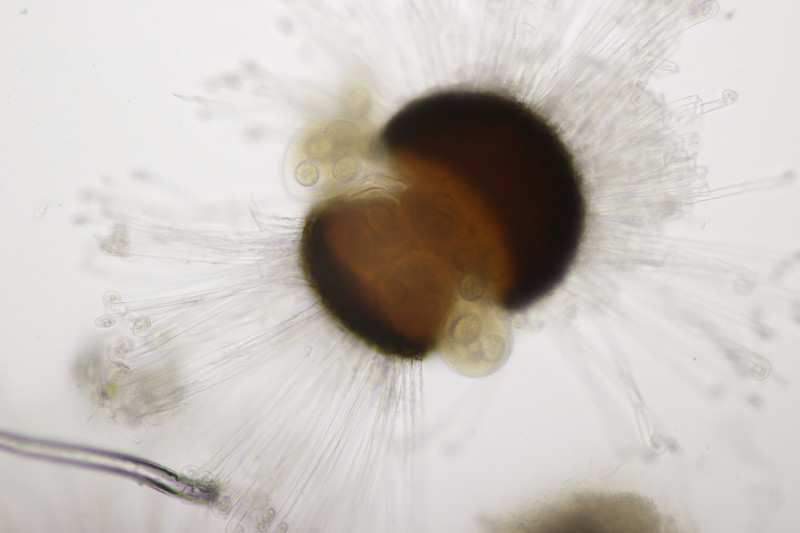

4. Uromyces geranii ex Geranium pratense












9. Gymnosporangium sabinae ex Pyrus sp.


5. Hier würde ich auf Mucilago crustacea tippen. Seltsamerweise waren keine Sporen zu sehen, nur Kalkkristalle




6. Dann war ich bei meinen Eltern, wo gegenüber ein Maisfeld ist. Dank Jules letztem Rundbrief wußte ich, daß die komische Pflanze, die an jedem Maisfeldrand wächst, Hühnerhirse ist und von einem Brandpilz (genauer sogar von 2 verschiedenen Bränden) befallen werden kann. Also sind meine 6-jährige Nichte und ich losgezogen und wurden auch schon bald fündig: Ustilago trichophora ex Echinochloa crus-galli
Gleispark Frintrop-0030.jpg










7. Mal wieder ein van Gogh unterm Mikroskop: Wilsoniana amaranthi ex Amaranthus sp.



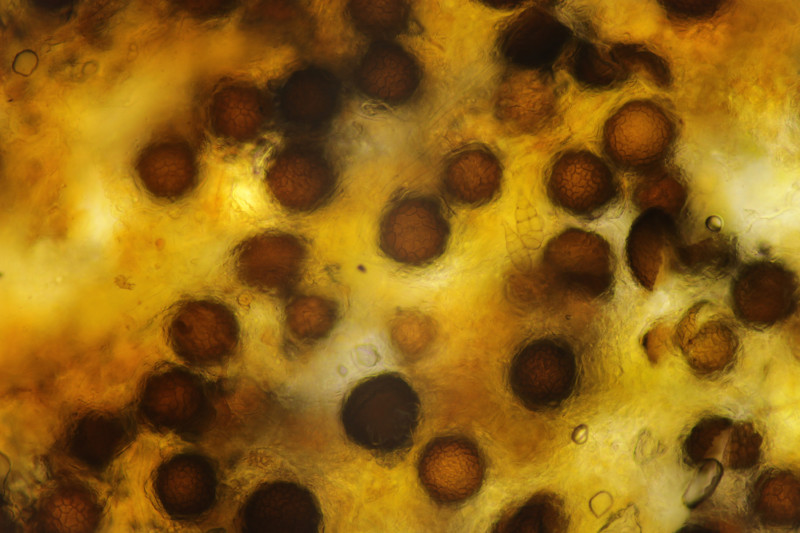
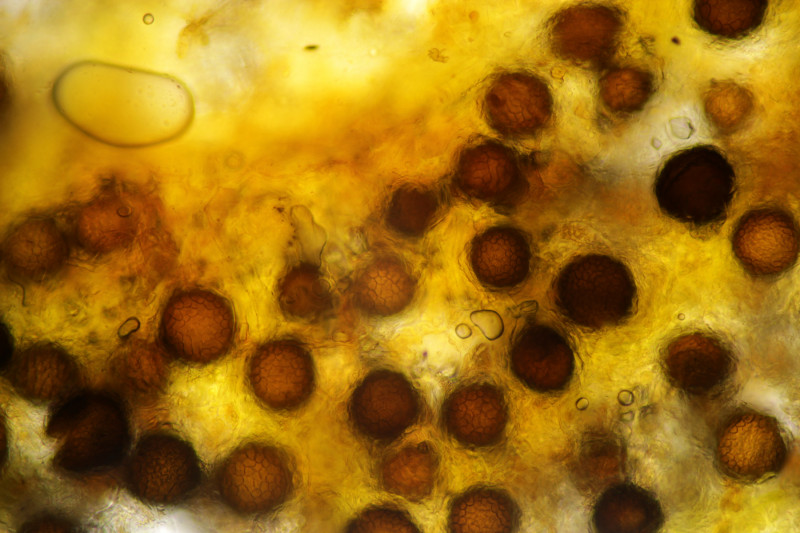
8. Und dann hat meine Mutter mir noch von ihrem Zitronenbaum erzählt, wo die Blätter abtrocknen und es kleine schwarze Beläge gibt. Unterm Mikroskop zeigten sich dann einerseits Alternaria-Sporen, andererseits auch diese Konidien hier. Viellecht hat da ja jemand eine Idee zu?
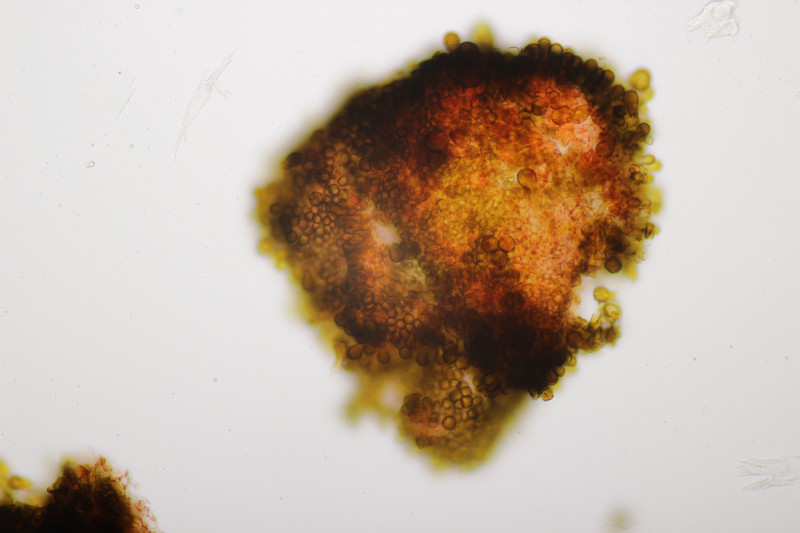
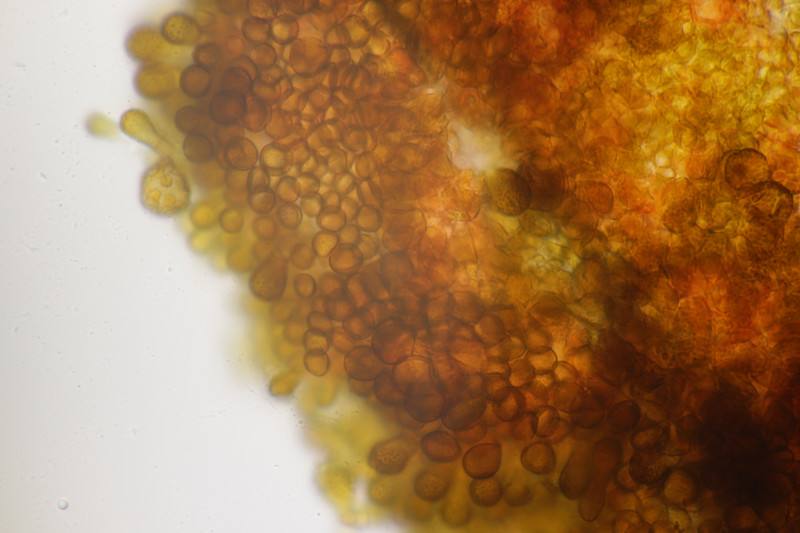

Björn


