Hallo zusammen,
am letzten Sonntag ging es mit dem APR beim strahlendem Sonnenschein zu einer Exkursion auf die Halde Hoppenbruch. Das Wetter hatte auch etliche Neulinge angelockt, so daß wir mit geschätzt 25 Leuten loszogen. Aber neben vielen Teilnehmer:innen gab es auch etliche Pilze:
1. Puccinia phyllostachydis ex Phyllostachys sp. Der einzige bekannte Fundort dieses Pilzes, der an den septierten Paraphysen der Uredien gut erkennbar ist.


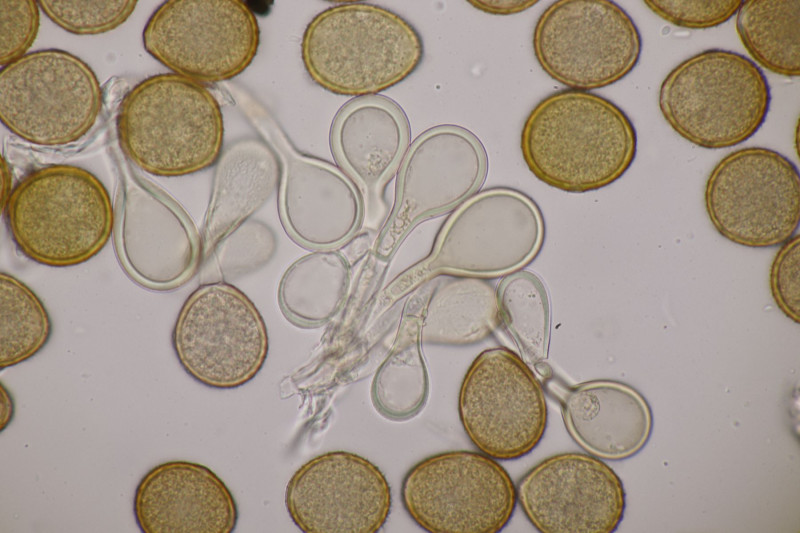
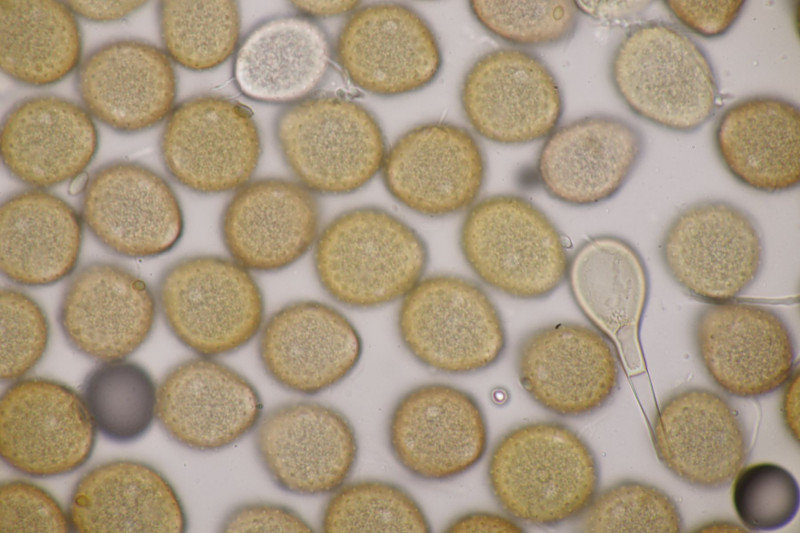

2. Tomentella bryophila, leicht kenntlich am amyloiden Apikulus




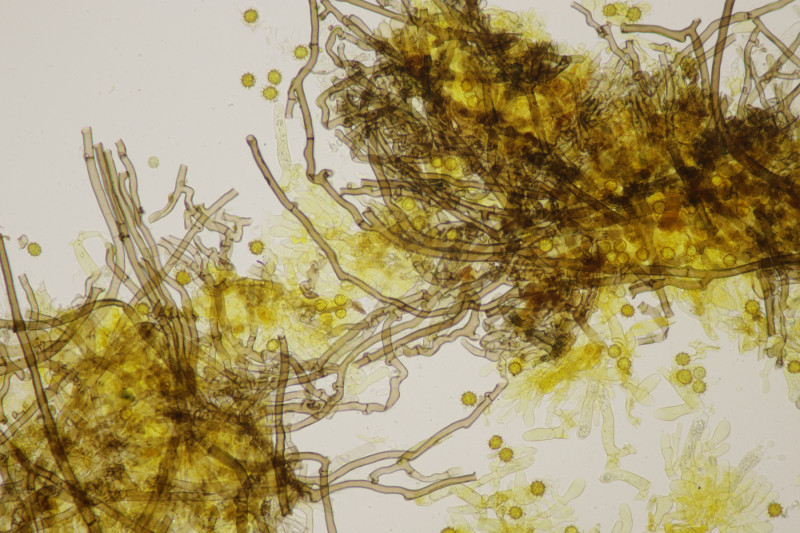
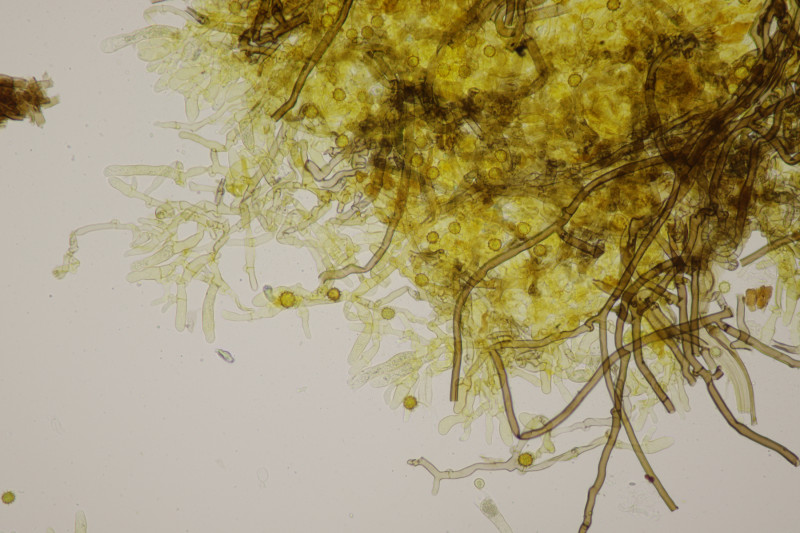



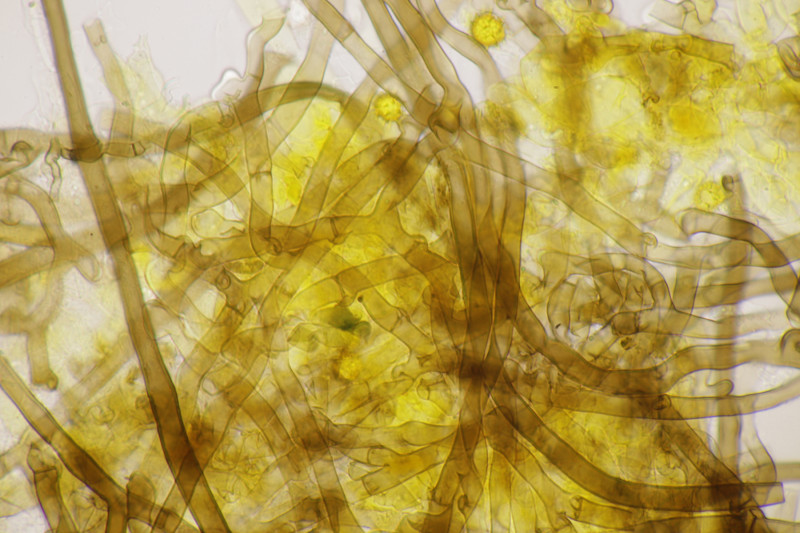

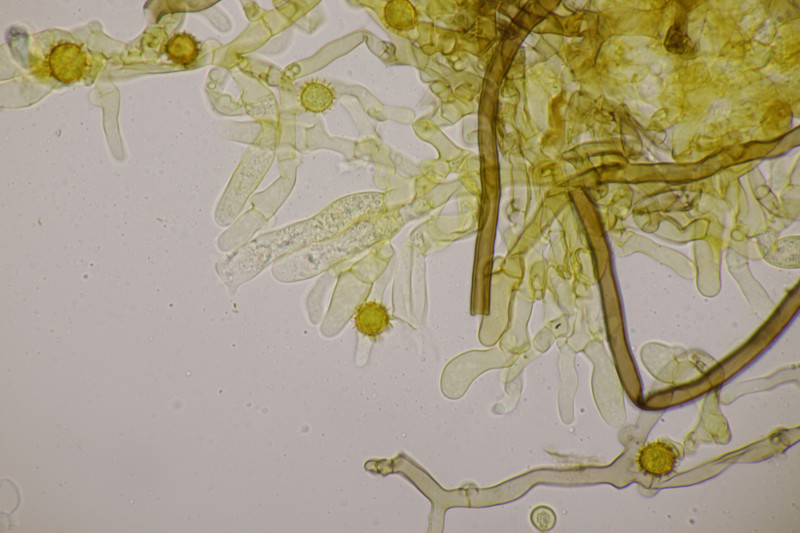

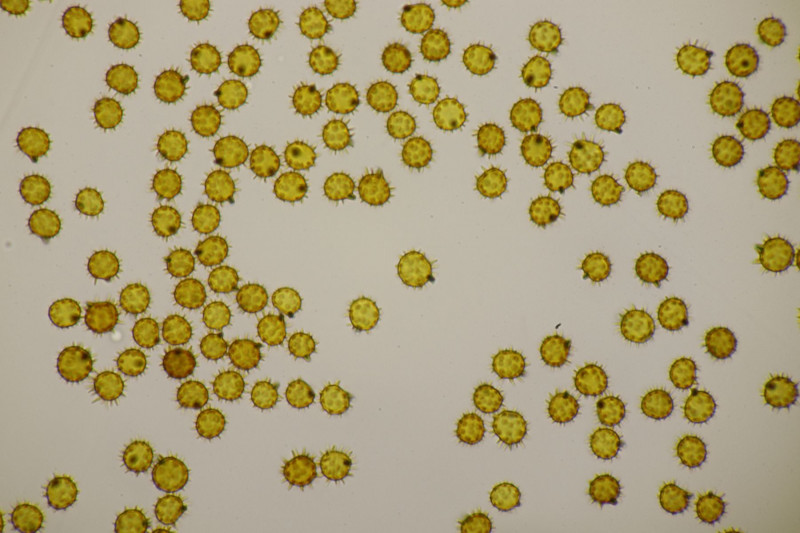
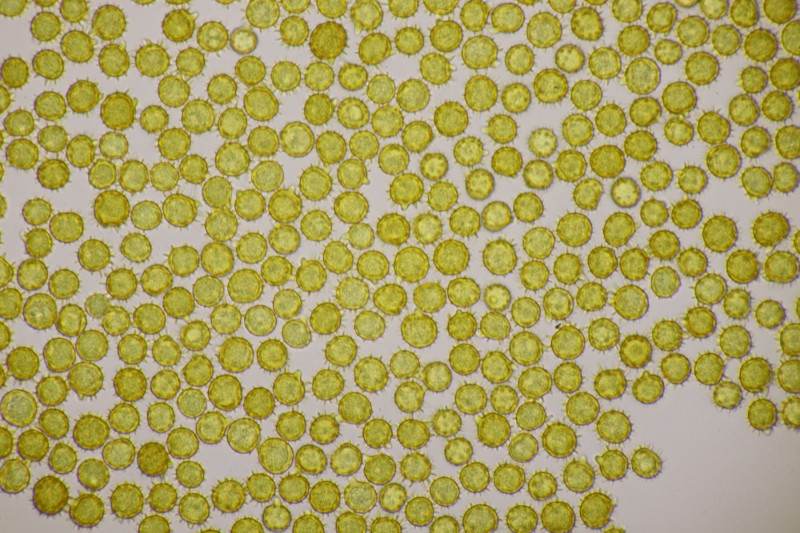

3. Lindtneria panphyliensis (oder eben L. bryophila, wenn man beides zu einer Art zusammenwirft)





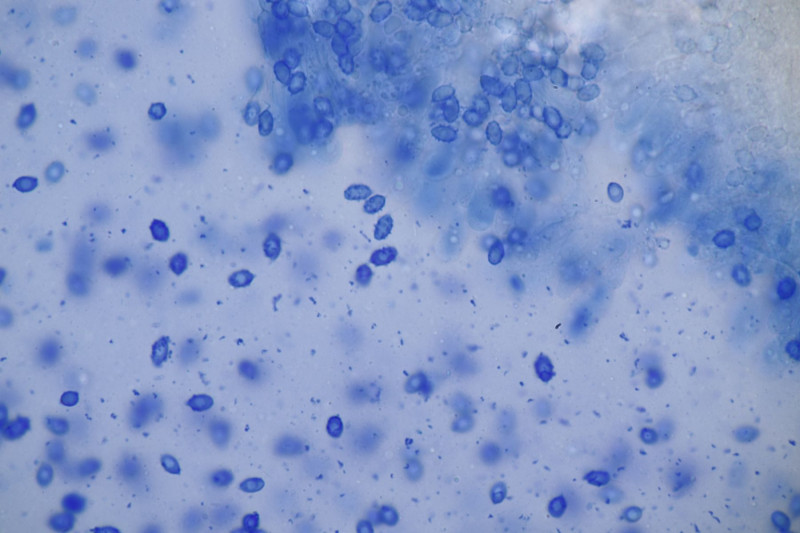
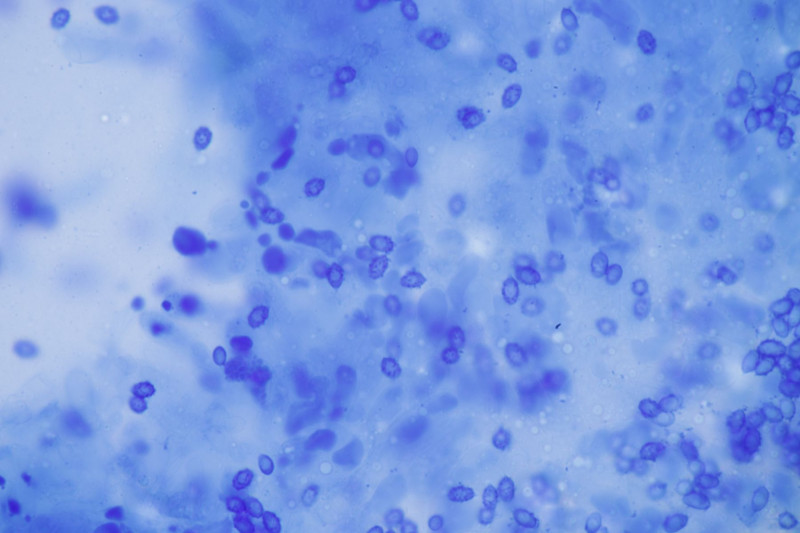
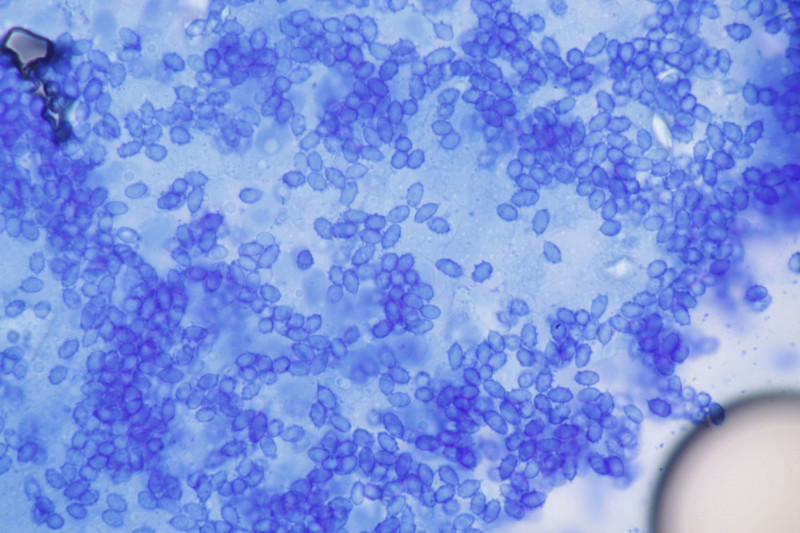
4. Phallus impudicus

5. Hypomyces stephanomatis an Geoglossum cookeanum. Normalerweise ist der Pilz an Humaria zu finden.

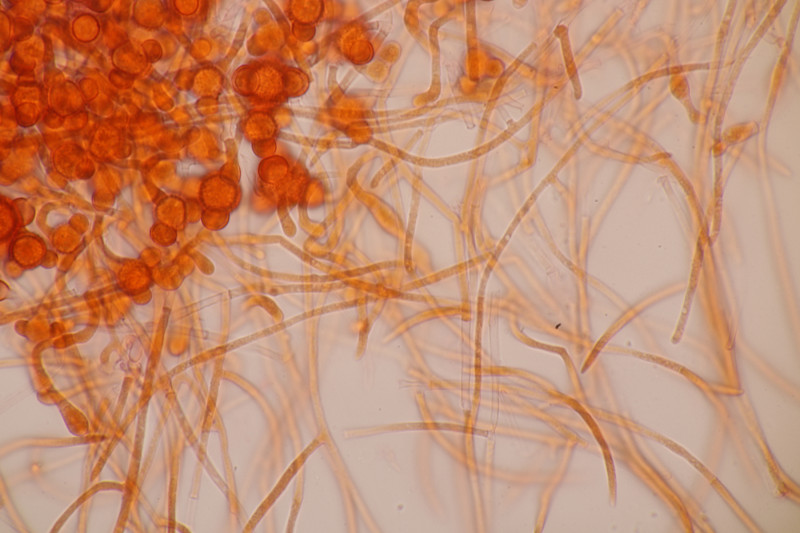

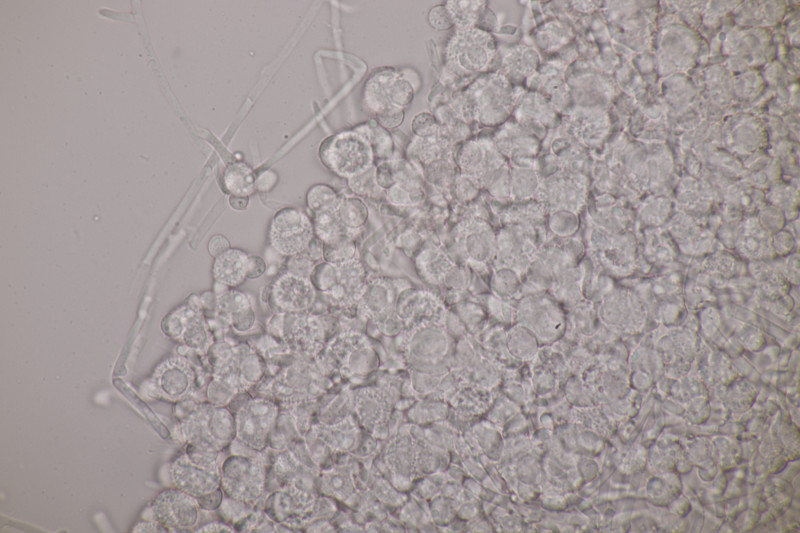
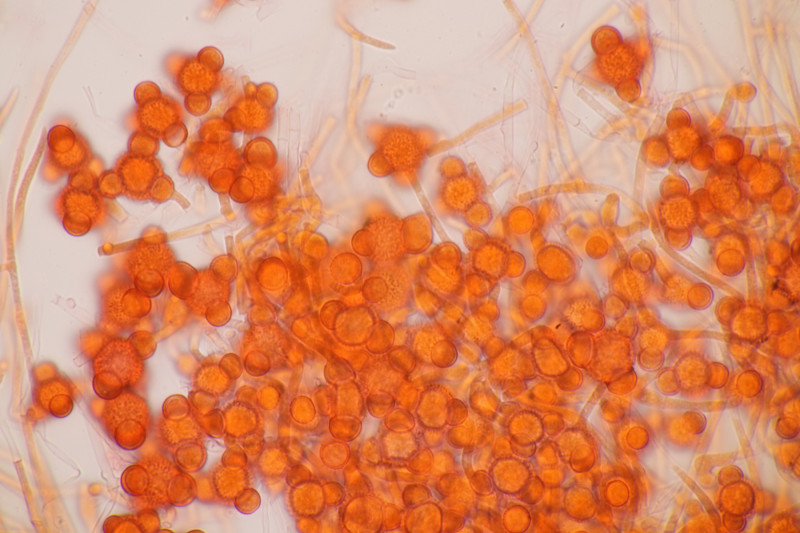
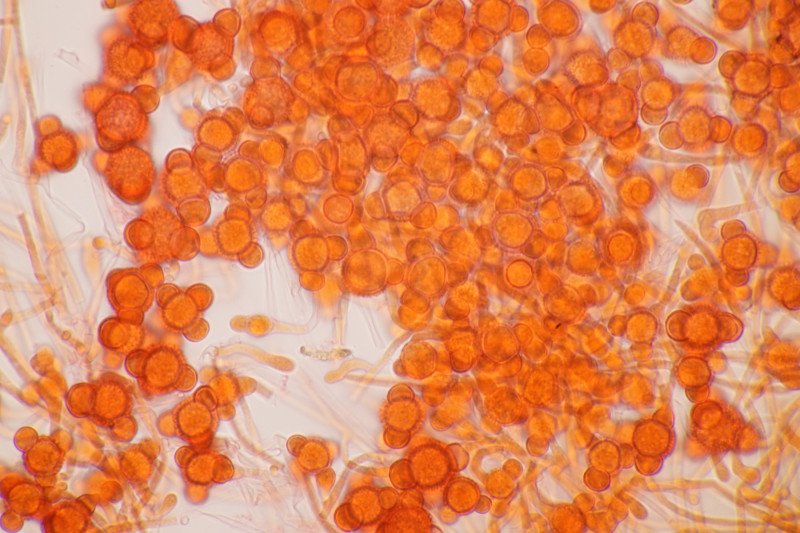

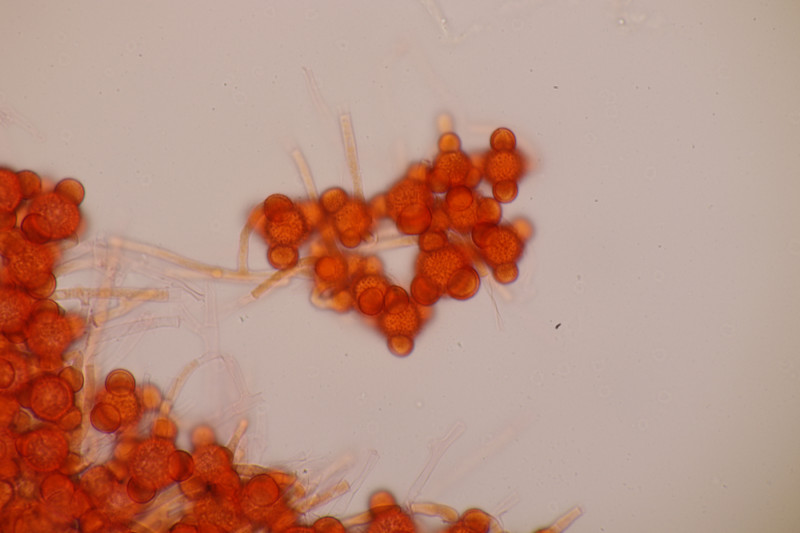
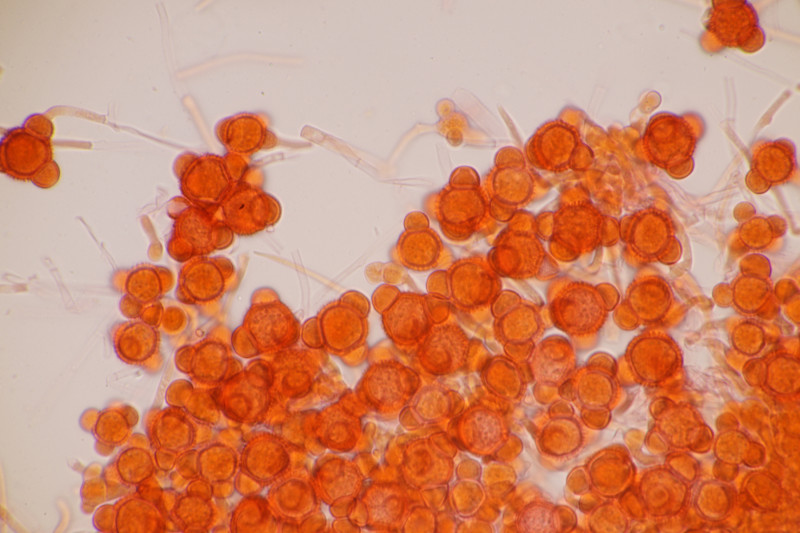
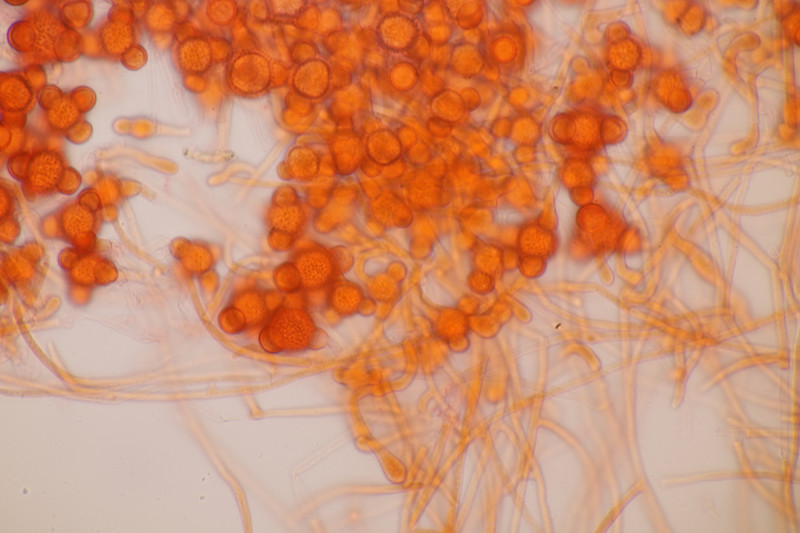
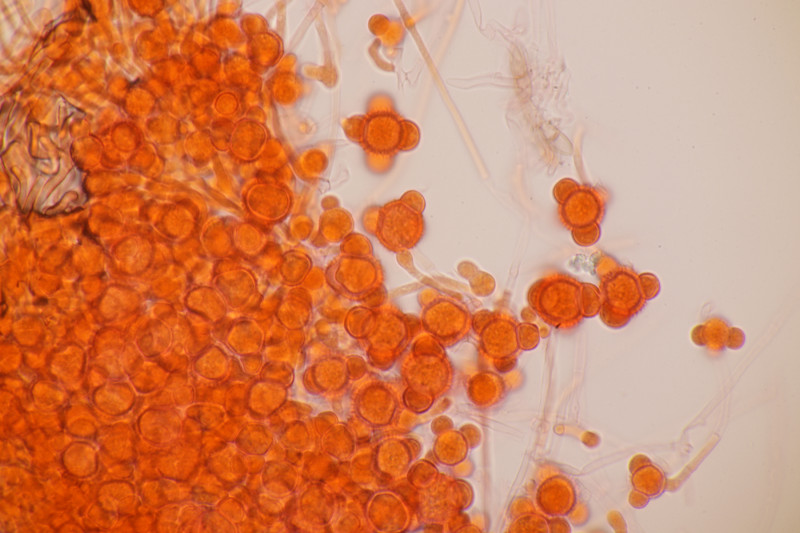
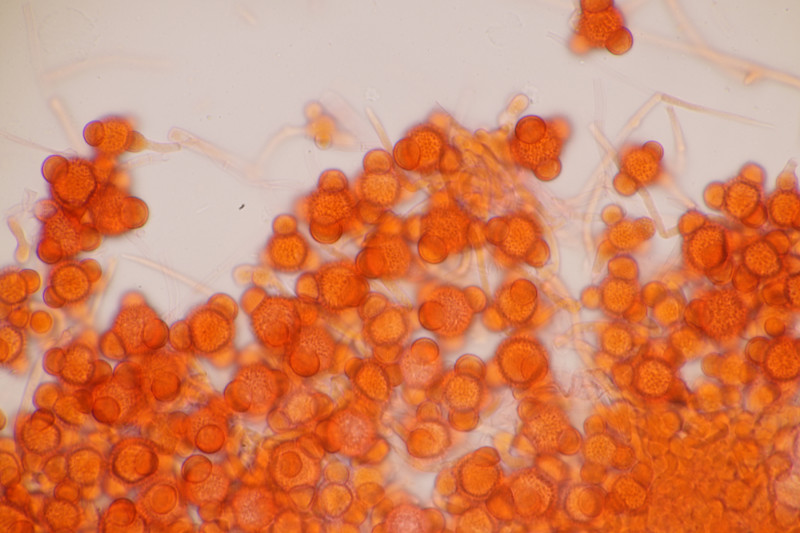
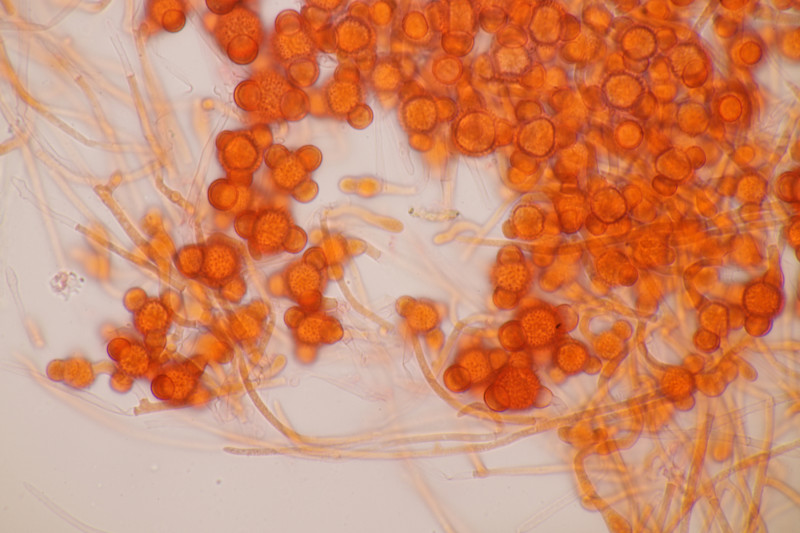
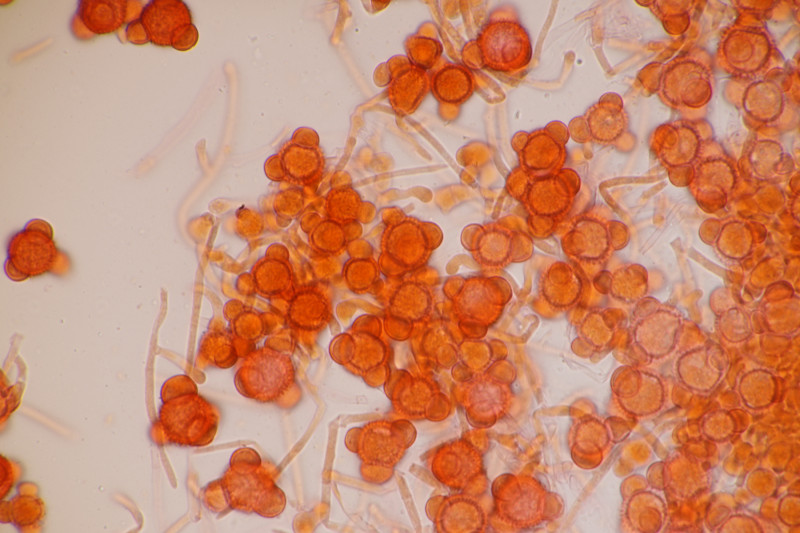

6. Geoglossum cookeanum


7. Eine Helvella... früher hätte man einfach H. lacunosa dazugesagt.


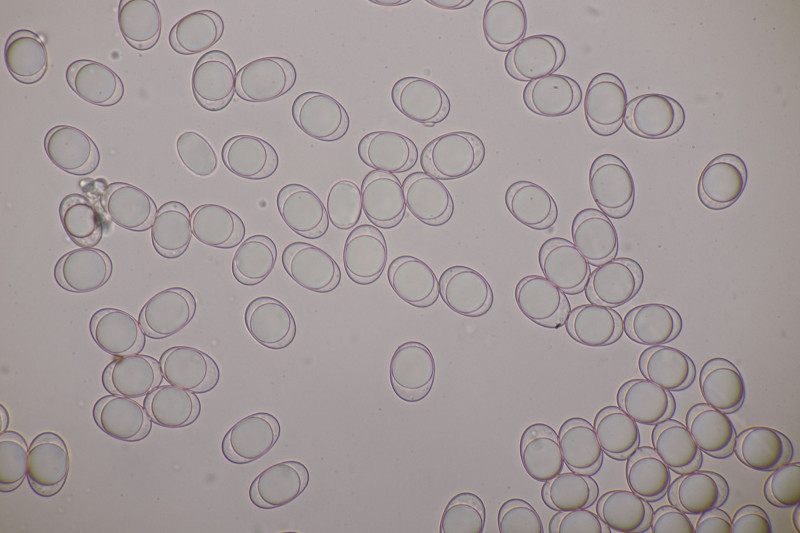


8. Erysiphe syringae-japonicae ex Ligustrum vulgaris


9. Helvella crispa

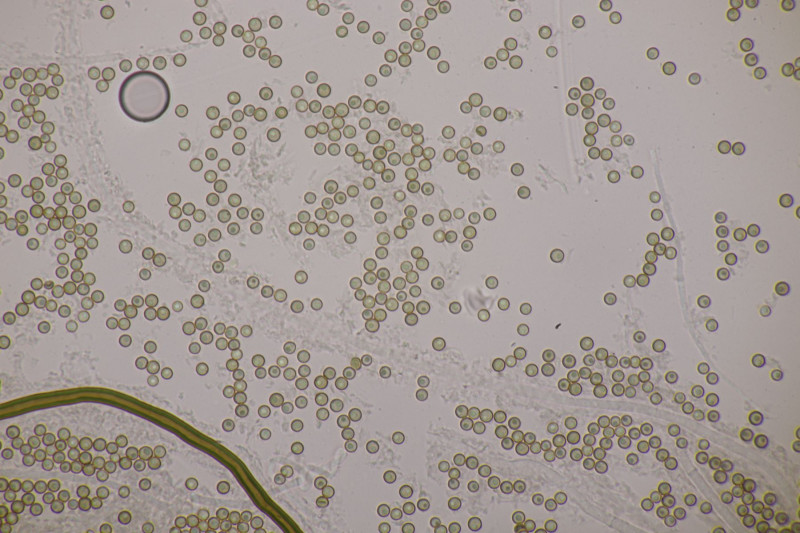
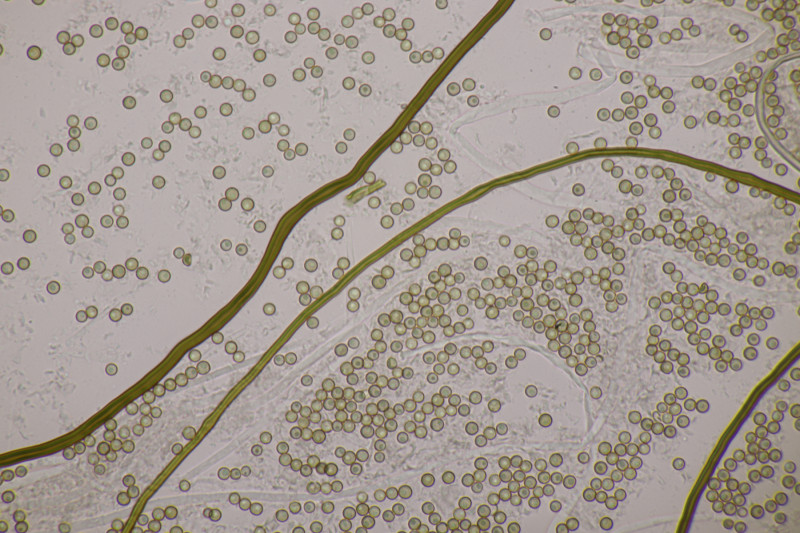
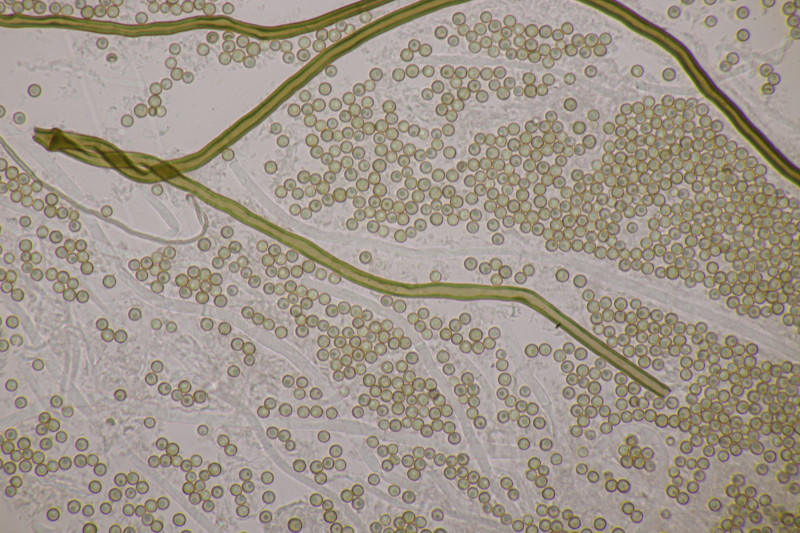
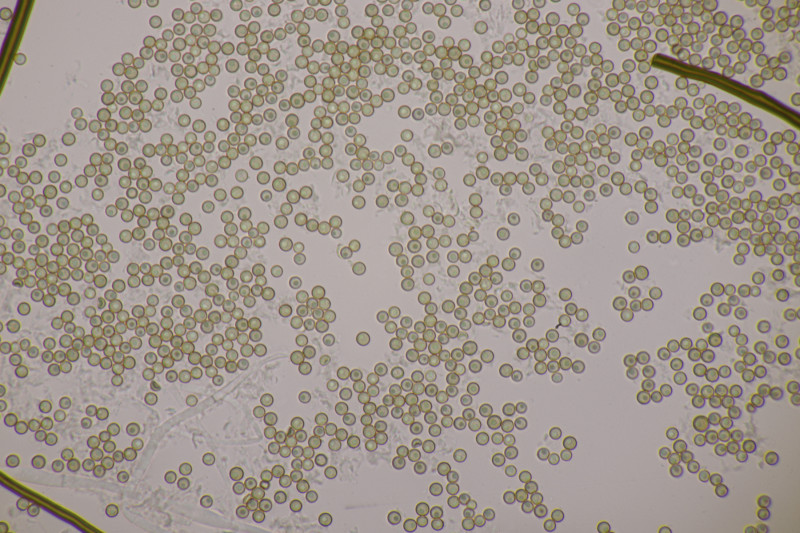
10. Hier haben wir im Feld gerätselt, was das für seltsame Stäublinge sein mögen. Mikroskopisch zeigte sich dann ein Capillitium ohne Poren und Septen, mit Paracapillitium untermischt, dazu praktisch glatte Sporen ohne Pedicel von 3,1-3,8 µm Durchmesser. Also Apioperdon pyriforme.

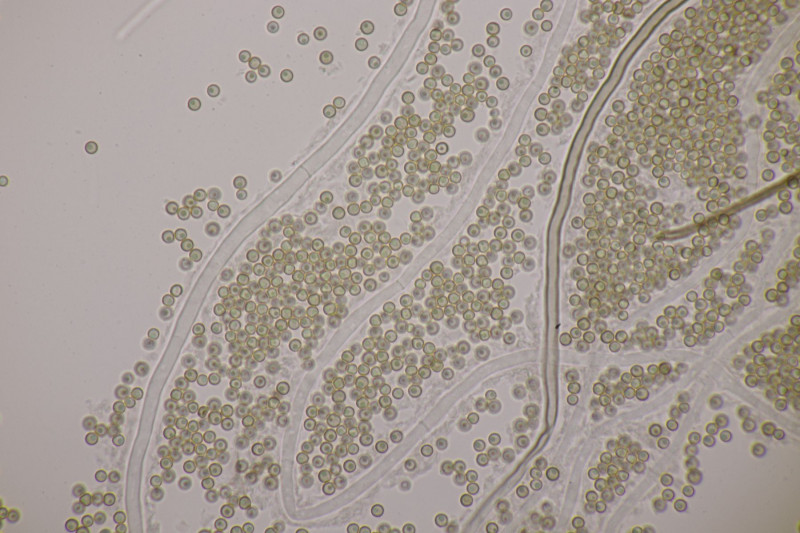
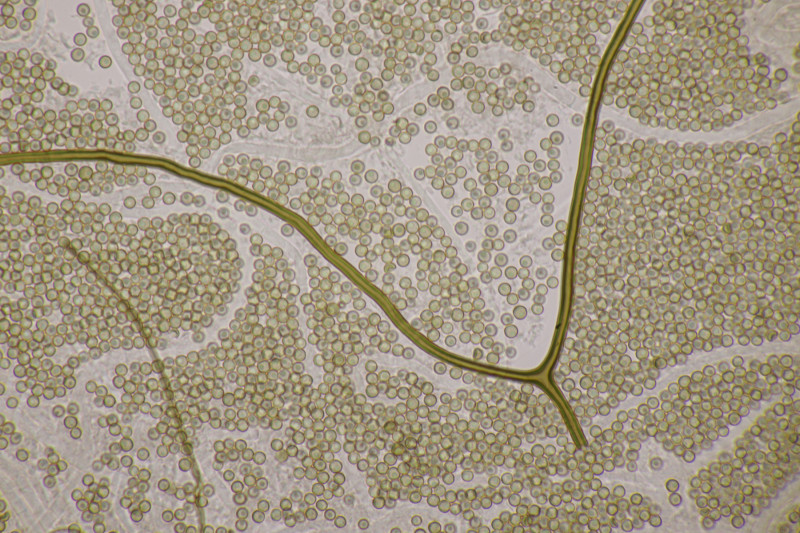
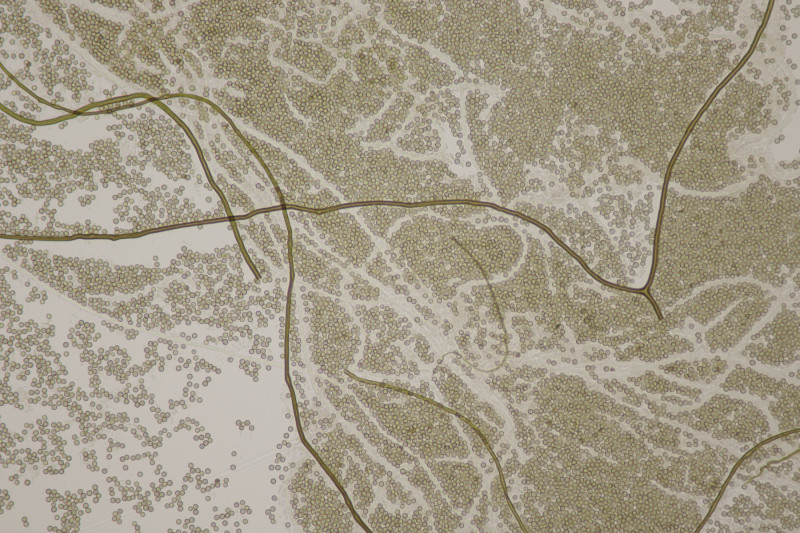
11. Eine Teilnehmerin fand dann diesen Käfer mit Beauvaria bassiana



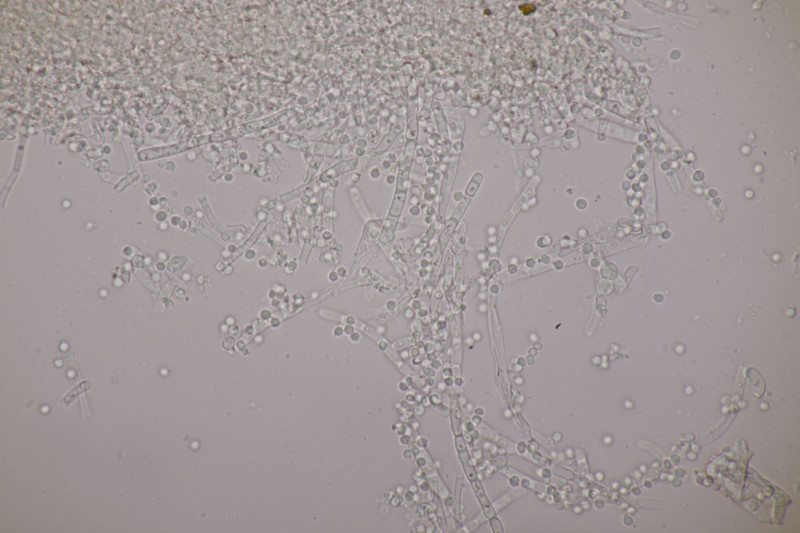
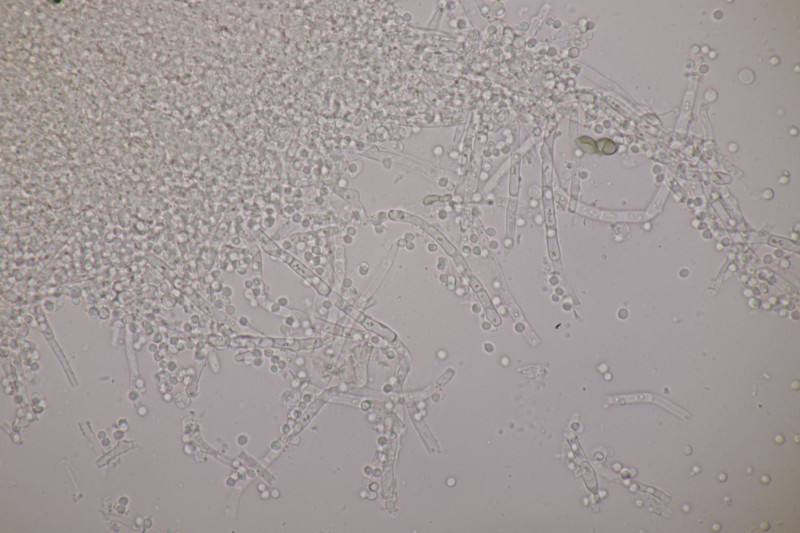
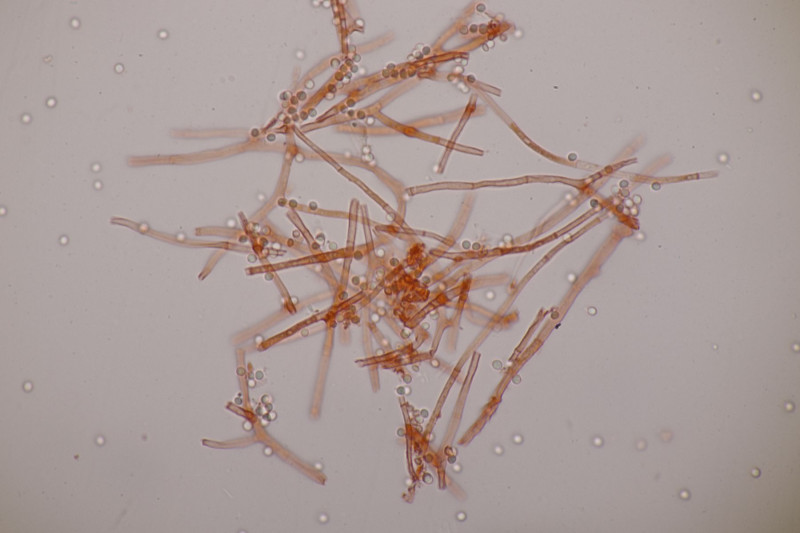

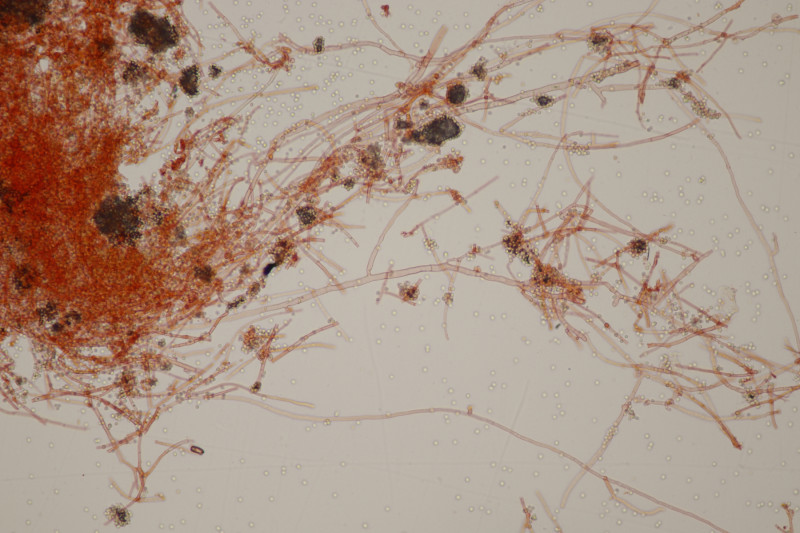


12. Sawadaea bicornis ex Acer pseudoplatanus für Tuppie



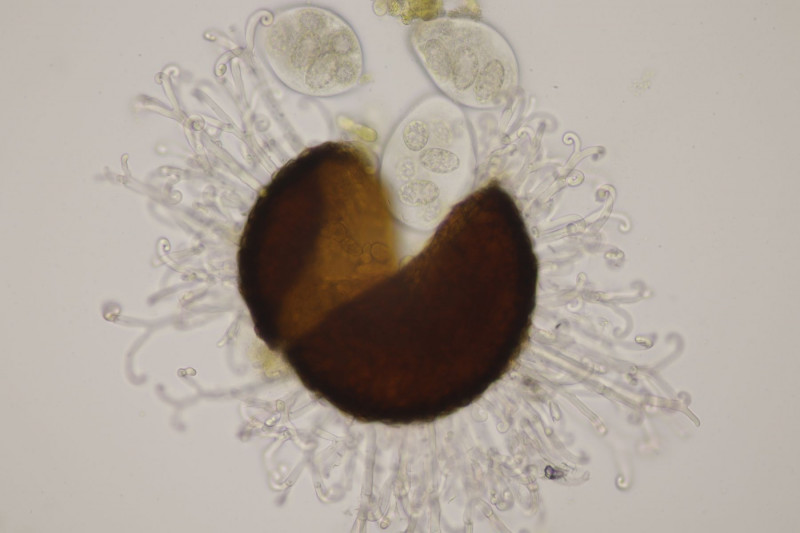

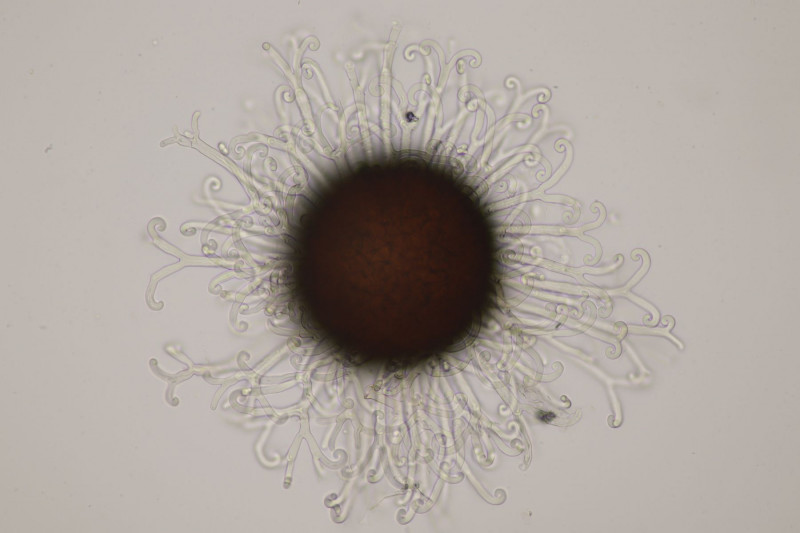
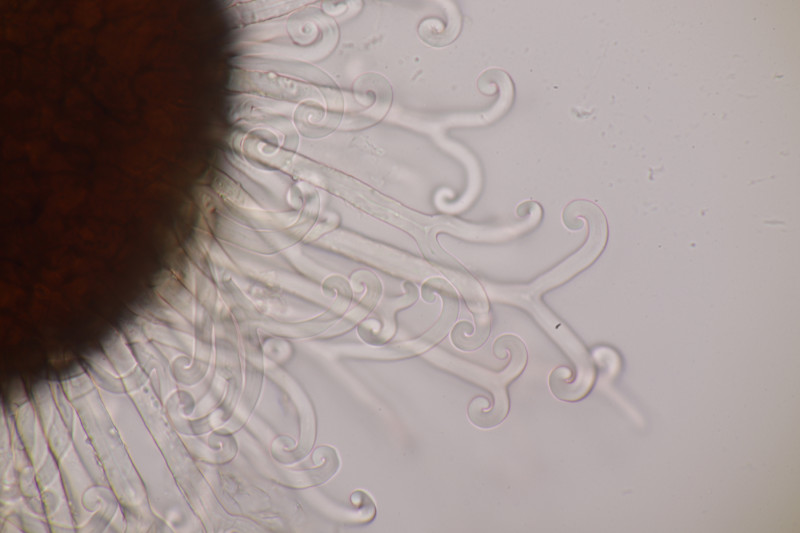



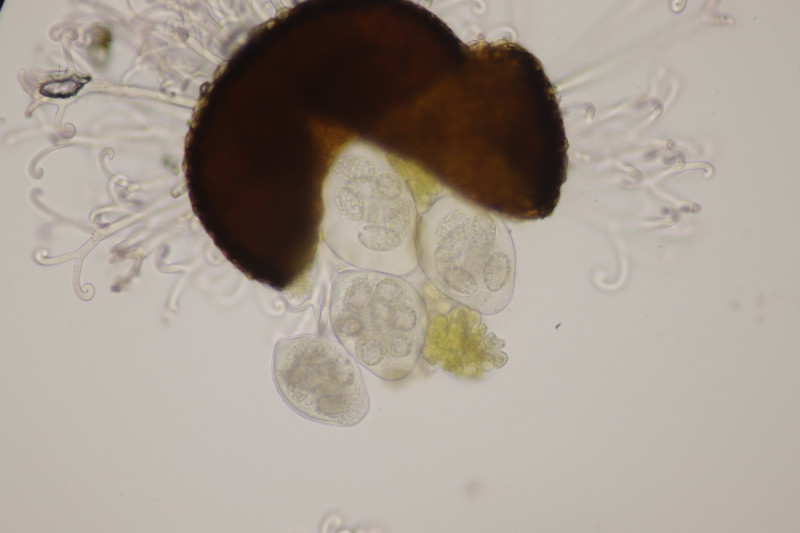
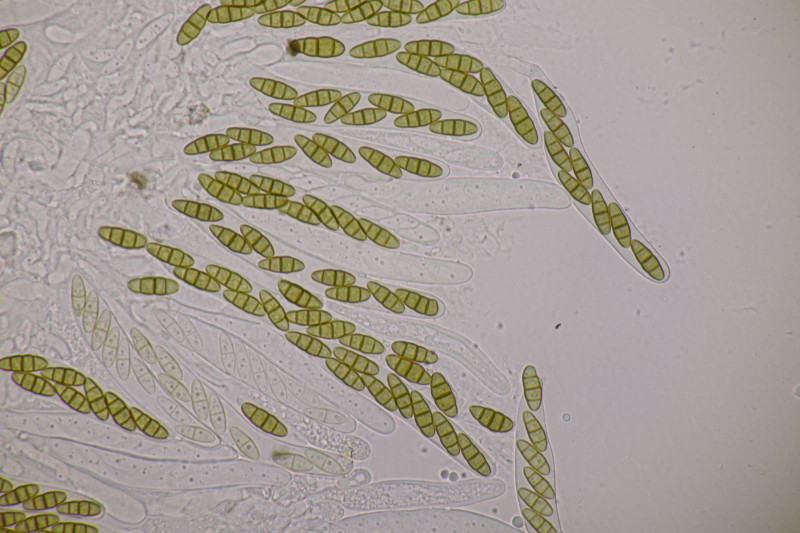
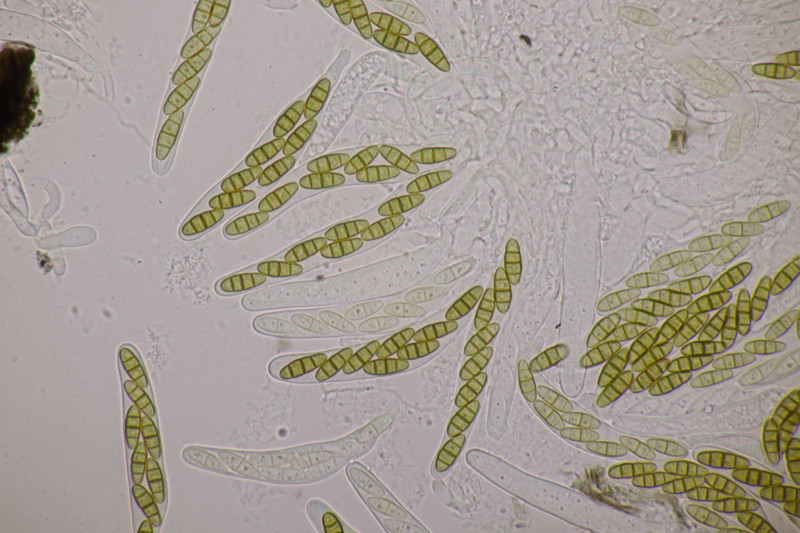
13. Mytilinidion decipiens
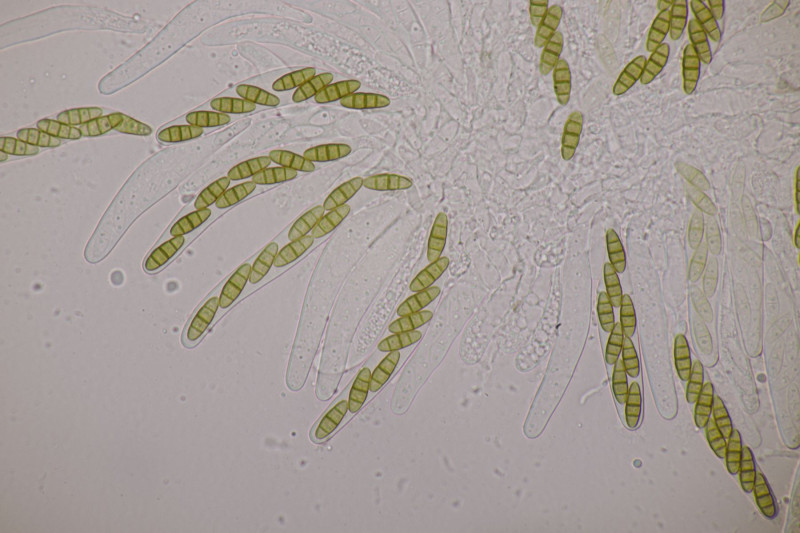
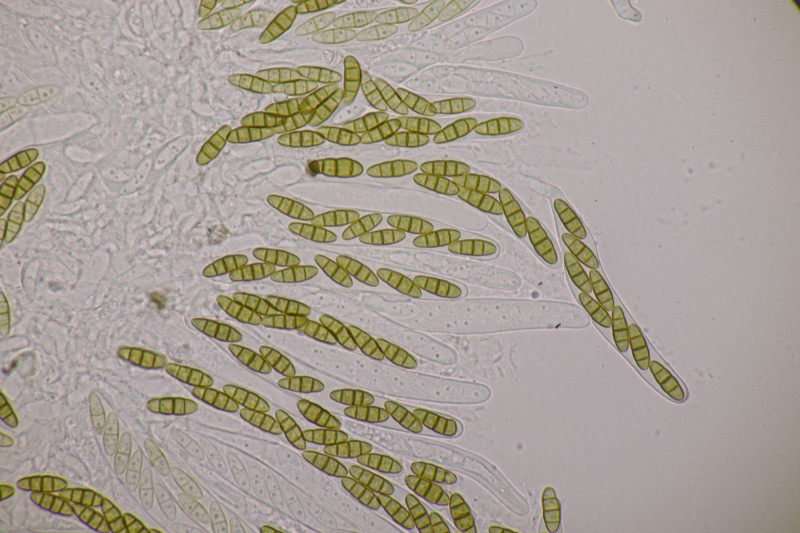
Björn


